
����Ŀ���鼰�仯������;�dz��㷺���ش��������⣺
(1)������ͬ���壬ԭ���������״�18������λ�����ڱ���________����__________�塣
(2) H3AsO3(������)������Ԫ���ᣬ��һ���͵ڶ�������ͨ����ˮ�е����������ʵ�ֵģ���������ֱ�ӵ����H+����һ�����뷽��ʽΪ��H3AsO3+H2O![]() [As(OH)4]-+H+���ڶ����ĵ��뷽��ʽΪ______________��
[As(OH)4]-+H+���ڶ����ĵ��뷽��ʽΪ______________��
(3)�Ŵ����������塷�ᴿ��˪�����������������������û��ϣ�������֮���������Ϸɣ��Ÿ����������ᣬ��Ȼ�´�����������������ᴿ�õĻ�������______________��������������˪(As2O3)���������ư�Ѫ�����������(FeAsS)���տ�������˪�ͺ���ɫ���壬�÷�Ӧ�Ļ�ѧ����ʽΪ__________________��
���𰸡� �� VA [As(OH)4]-+H2O![]() [As(OH)5]2-+H+ ���� 2FeAsS+5O2
[As(OH)5]2-+H+ ���� 2FeAsS+5O2 ![]() Fe2O 3+As2O3+2SO2
Fe2O 3+As2O3+2SO2
��������������Ҫ��������ͬ������鼰�仯����
(1)������ͬ���壬ԭ���������״�18��������λ�����ڱ��������ڡ�VA��������������������Ԫ��ԭ���������18������λ�����ڱ��������ڡ�VA�塣
(2) H3AsO3(������)������Ԫ���ᣬ��һ���͵ڶ�������ͨ����ˮ�е����������ʵ�ֵģ���������ֱ�ӵ����H+����һ�����뷽��ʽΪ��H3AsO3+H2O![]() [As(OH)4]-+H+���ڶ����ĵ��뷽��ʽΪ[As(OH)4]-+H2O
[As(OH)4]-+H+���ڶ����ĵ��뷽��ʽΪ[As(OH)4]-+H2O![]() [As(OH)5]2-+H+��
[As(OH)5]2-+H+��
(3)���������Ϸ���ָ��˪���������Ÿ����������ᡱָ��˪���������ᴿ�õĻ����������������������(FeAsS)���տ�������˪�ͺ���ɫ���壬��Ԫ��ת��Ϊ����ɫ��������������Ԫ��ת��Ϊ����������Ԫ��ת��Ϊ��˪���÷�Ӧ�Ļ�ѧ����ʽΪ2FeAsS+5O2 ![]() Fe2O 3+As2O3+2SO2��
Fe2O 3+As2O3+2SO2��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в�����ٽ�ˮ�ĵ��룬��ʹ��ҺpH>7����( )
A������ˮ���ȵ�90 �� B����ˮ�м�������NaOH
C����ˮ�м�������Na2CO3 D����ˮ�м�������FeCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʼ��ת����Ҫ���Ƿ�Ӧʵ�ʡ������Լ����ʵ���������������ת���ڸ�����������ʵ�ֵ���
��Si ![]() SiO2
SiO2 ![]() H2SiO3 ��S
H2SiO3 ��S ![]() SO2
SO2 ![]() H2SO4
H2SO4
��C ![]() CO2
CO2 ![]() Na2CO3 ��NaCl��Һ
Na2CO3 ��NaCl��Һ![]() NaCl����
NaCl����![]() Na
Na
��Na ![]() Na2O
Na2O![]() NaOH ��HCl(Ũ)
NaOH ��HCl(Ũ) ![]() Cl2
Cl2![]() Ư��
Ư��
A. �٢ڢۢ� B. �ڢۢ� C. �٢ܢݢ� D. �ڢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þ����Ͻ�㷺Ӧ���ں��պ��졢��ͨ����ص���ҵ��
��֪��CaO(s)+3C(s)=CaC2(s)+CO(g) ��H= +464 kJ��mol-1
MgO(s)+ CaC2(s)=CaO(s)+ Mg(g)+2C(s) ��H =+177.5 kJ��mol-1
(1)þ�����ڶ�����̼��ȼ�գ�д����ѧ��Ӧ����ʽ_____________________��
(2)д��MgO(s)��C(s)����1 mol CO(g)����̬þ���Ȼ�ѧ����ʽ��________________��
(3) �õ�ⷨ��ȡþʱ����ԭ���Ȼ�þ����ˮʱ���ڵ���¶��£�ԭ�ϻ��γ�Mg(OH)Cl�����������뷴Ӧ��Mg(OH)Cl=Mg(OH)++Cl-�����ʱ������������������þ�ۻ�Ĥ����ʱ�����ķ�ӦʽΪ________________��
(4)þ/�����������ع���ʱþת��Ϊ������þ�������������ת��Ϊ����������������������������Ľṹ��ʽ��þ/�����������ص�װ�����£�
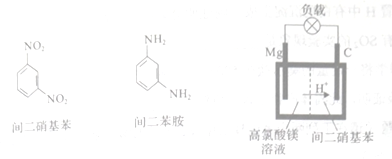
�õ�طŵ�ʱ��������Ӧ����ʽΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����еݱ������ȷ����
A. �ȶ��ԣ�HBr< HF B. ��ԭ�ԣ�S2�C< Cl�C
C. �е㣺����>���� D. ���ԣ�HIO4> HClO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���ˮ��Һ��1molCl����ClOx��(x=1��2��3��4)������(kJ)��Դ�С��ͼ��ʾ�������й�˵����ȷ���ǣ� ��

A. a��b��c��d��e�У�c���ȶ�
B. b��a+c��Ӧ�Ļ��Ϊ20kJ��mol��1
C. b��a+d��Ӧ���Ȼ�ѧ����ʽΪ3ClO��(aq)=ClO3��(aq)+2Cl��(aq) ��H=+116kJ��mol��1
D. һ���¶��£�Cl2��NaOH��Һ��Ӧ���ɵIJ�����a��b��d����Һ��a��b��d��Ũ��֮�ȿ���Ϊ11��1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����Ľ���Cu��ȫ��������Ũ�����У��ռ���������壨��NO��N2O4��NO2����1.8 mol������������ƽ����Ϊ���ݣ�һ�����״����8.96LO2��Ϻ���ˮ���գ�������ʣ�ࣻ��һ��ǡ���ܱ�500mL 2mol/L NaOH��Һ��ȫ���գ����ɺ�NaNO3��NaNO2������Һ��������NaNO3�����ʵ���Ϊ
A. 0.1mol B. 0.15mol C. 0.2mol D. 0.25mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��Q��Ԫ�����ڱ��е����λ����ͼ��ʾ������˵������ȷ����

A. Ԫ��W������������Ӧˮ��������Ա�Q��ǿ
B. ԭ�Ӱ뾶�Ĵ�С˳��Ϊ��r(W2-)��r(Q-)��r(Y2-)> r(Z3+)
C. Ԫ��X��Q���⻯�ﻯ�ϵIJ����мȺ����ۼ��ֺ����Ӽ�
D. X��Z��W��Q����Ԫ�ص�����������Ӧˮ���������ǿ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɫ��ѧ���Ի�ѧ��Ӧ����ˡ�ԭ�Ӿ����ԡ���ԭ�ӽ�Լ���ĸ��Ҫ�������ԭ�Ӿ����Է�Ӧ��ԭ�Ϸ����е�����ԭ��ȫ��ת��������������������ʵ�����ŷš����·�Ӧ�з��ϡ���ɫ��ѧ������( )
A. �Ա����Ҵ�Ϊԭ�ϣ���һ�������������ұ�
B. ����������������Ӧ���Ʊ�������
C. ��ϩ�����������Ĵ����������ɻ�������(�ṹ��ʽ��ͼ)
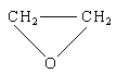
D. �Ҵ���Ũ���Ṳ���Ʊ���ϩ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com