
【题目】某可逆反应平衡常数表达式为K=![]() 达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小.下列说法正确的是
达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小.下列说法正确的是
A.反应的热化学方程式为NO2(g)+SO2(g) ![]() NO(g)(g)+SO3(g) △H>0
NO(g)(g)+SO3(g) △H>0
B.一定条件下达到平衡时,缩小容器体积,增大体系压强,气体颜色加深
C.混合气体的平均摩尔质量保持不变,说明反应已达平衡
D.使用合适的催化剂可使该反应的反应速率和平衡常数增大
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质的性质类比正确的是( )
A. 已知Fe+S![]() FeS,则Cu+S
FeS,则Cu+S![]() CuS
CuS
B. Fe能与CuSO4溶液反应,可知Al与CuSO4溶液也能反应
C. CaSO3与稀盐酸反应生成SO2,可知CaSO3与稀硝酸反应也生成SO2
D. 已知H2O2能氧化I-,可知H2O2也能氧化Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇脱氢可制取甲醛:CH3OH(g)![]() HCHO(g)+ H2(g), 甲醇的平衡转化率随温度变化的曲线如右图所示(已知反应在IL 的密闭容器中进行)。下列有关说法正确的是( )
HCHO(g)+ H2(g), 甲醇的平衡转化率随温度变化的曲线如右图所示(已知反应在IL 的密闭容器中进行)。下列有关说法正确的是( )
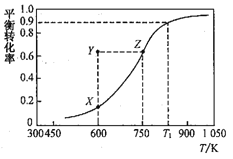
A. 平衡常数:K600K<K750K
B. 从Y到Z点可通过增大压强实现
C. 在TlK时,该反应的平衡常数为8.1
D. 若工业上利用此反应进行生产,为了提高经济效益将反应温度升高至1050K以上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,但存在溶解平衡.当达到平衡时,溶液中离子浓度的乘积是一个常数(此常数用Ksp表示,Ksp和水的KW相似).如:
AgX(s)![]() Ag+(aq)+X-(aq);Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
Ag+(aq)+X-(aq);Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
AgY(s)![]() Ag+(aq)+Y-(aq);Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
Ag+(aq)+Y-(aq);Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
AgZ(s)![]() Ag+(aq)+Z-(aq);Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
Ag+(aq)+Z-(aq);Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(用已被溶解的溶质的物质的量/1 L溶液表示)S(AgX)、S(AgY)、S(AgZ)的大小顺序为 。
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-) (填“增大”、“减小”或“不变”)。
(3)在25℃时,若取0.188 g的AgY(相对分子质量为188)固体放入100 mL水中(忽略溶液体积的变化),则溶液中Y-的物质的量浓度为 。
(4)①由上述Ksp判断,在上述(3)的体系中,能否实现AgY向AgZ的转化,并简述理由: ②在上述(3)体系中,能否实现AgY向AgX的转化?根据你的观点选答一项.若不能,请简述理由: ,若能,则实验转化的必要条件是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铜粉加入到100mL某浓度的稀硝酸中,充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体a mL(标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器中仍剩有铜粉m2g,则(m1-m2)为
A. ![]() B.
B. ![]() C.0 D.缺少条件,无法计算
C.0 D.缺少条件,无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体体积的大小与许多因素有关。当温度和压强一定时,气体体积主要取决于( )
A.气体的种类 B.气体的物质的量
C.气体分子本身的大小 D.气体分子之间的平均距离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用pH试纸测定某溶液的pH,如果先将pH试纸用蒸馏水润湿后,再把待测液滴到pH试纸上,跟比色 卡对照,溶液的pH测得值为8,则该溶液的实际pH( )
A.大于8 B.小于8 C.等于8 D.小于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.金属氧化物一定是碱性氧化物 B.碱性氧化物一定是金属氧化物
C.非金属氧化物一定是酸性氧化物 D.酸性氧化物一定是非金属氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右表是元素周期表的一部分,其中A、B、D、E、G、J为短周期元素,G元素的核电荷数为B元素的2倍。请回答下列问题:
A | B | ||
D | E | G | J |
L | M | Q |
(1)J的最高价氧化物对应水化物的化学式是___________________。
(2)G2J2常用作橡胶的低温硫化剂和黏结剂,其电子式为_______________________。写出一个能表示元素G、J非金属性强弱关系的化学方程式____________________________。
(3)G单质在空气中燃烧生成一种无色有刺激性气味的气体,该无色有刺激性气味的气体与含1molJ的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在—定条件下反应,可生成一种强酸和一种氧化物,且该反应中有NA个电子转移,则该反应的化学方程式是________________________。
(4)A的最简单氢化物是___________(填“极性”或“非极性”)分子,实验室制备该物质的化学方程式为__________________________________________。
(5)根据元素周期律,可以推测上表中长周期元素的单质具有半导体特性的是__________(填元素符号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com