
����Ŀ������![]() ������������ϩ�����ȶ�����
������������ϩ�����ȶ�����![]() ���Ͽ�ʼʧȥ�ᾧˮ��������ˮ���л��ܼ�����Ǧ��
���Ͽ�ʼʧȥ�ᾧˮ��������ˮ���л��ܼ�����Ǧ��![]() ��Ҫ�ɷ�ΪPbO��Pb��
��Ҫ�ɷ�ΪPbO��Pb��![]() ��
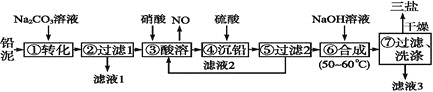
��![]() Ϊԭ���Ʊ����εĹ���������ͼ��ʾ��
Ϊԭ���Ʊ����εĹ���������ͼ��ʾ��
��֪��![]() ��
��![]() ���ܽ�Ⱥ��ܶȻ�Ksp���±���
���ܽ�Ⱥ��ܶȻ�Ksp���±���
������ |
|
|
�ܽ�� |
|
|
Ksp |
|
|
(1)����![]() ת����Ŀ����___ ����Һ1�е�����Ϊ
ת����Ŀ����___ ����Һ1�е�����Ϊ![]() ��____
��____![]() �ѧʽ
�ѧʽ![]() ��
��
(2)����![]() ����ʱ��Ϊ����������ʣ��ɲ�ȡ�Ĵ�ʩ��____
����ʱ��Ϊ����������ʣ��ɲ�ȡ�Ĵ�ʩ��____![]() ��дһ��
��дһ��![]() ������Ǧ�����ᷴӦ����
������Ǧ�����ᷴӦ����![]() ��NO�����ӷ���ʽΪ_______��
��NO�����ӷ���ʽΪ_______��
(3)��Һ2�п�ѭ�����õ����ʵĻ�ѧʽΪ____��������![]() ��Ǧ�����Һ��
��Ǧ�����Һ��![]() �����ʱ
�����ʱ![]() _____
_____![]() ��
��
(4)����![]() �ϳ����εĻ�ѧ����ʽΪ__________________��
�ϳ����εĻ�ѧ����ʽΪ__________________��
���𰸡���![]() ת��Ϊ
ת��Ϊ![]() ���Ǧ��������
���Ǧ�������� ![]() �ʵ�����
�ʵ�����![]() ���ʵ���������Ũ�Ȼ��С����������
���ʵ���������Ũ�Ȼ��С����������![]() ��
�� ![]()
![]()
![]() 4PbSO4+6NaOH
4PbSO4+6NaOH![]() 3PbOPbSO4H2O+3Na2SO4+2H2O
3PbOPbSO4H2O+3Na2SO4+2H2O
��������
��200.0tǦ�ࣨ��Ҫ�ɷ�ΪPbO��Pb��PbSO4�ȣ�Ϊԭ���Ʊ����Σ���Ǧ���м�Na2CO3��Һ�ǽ�PbSO4ת����PbCO3��Na2CO3(aq)+PbSO4(s)=Na2SO4(aq)+PbCO3(s)��������Һ���������Ҫ��Na2SO4������Na2CO3��Pb��PbO��PbCO3������������·�Ӧ��3Pb+8HNO3=Pb(NO3)2+2NO��+4H2O��PbCO3+2HNO3=Pb(NO3)2+CO2��+H2O��PbO+2HNO3=Pb(NO3)2+2H2O����ת����Pb(NO3)2��Pb(NO3)2�м�ϡH2SO4ת����PbSO4�����ᣬ���˵���ҺΪHNO3����ѭ�����ã�������Ǧ�м����������ƺϳ����κ������ƣ�4PbSO4+6NaOH![]() 3PbOPbSO4H2O+3Na2SO4+2H2O����Һ3��Ҫ�������ƣ�ϴ�ӳ�������õ����Σ��ݴ˷������
3PbOPbSO4H2O+3Na2SO4+2H2O����Һ3��Ҫ�������ƣ�ϴ�ӳ�������õ����Σ��ݴ˷������
(1)�������Ǧ���м�Na2CO3��Һ���ɱ���֪PbCO3���ܽ��С��PbSO4���ܽ�ȣ�Na2CO3(aq)+PbSO4(s)=Na2SO4(aq)+PbCO3(s)����ɽ�PbSO4ת����PbCO3��������Һ���������Ҫ��Na2SO4������Na2CO3��
(2)����ʱ��Ϊ����������ʣ��ɲ�ȡ�Ĵ�ʩ���ʵ�����(���ʵ���������Ũ�Ȼ��С����������)��Ǧ�����ᷴӦ����Pb(NO3)2��NO�����ӷ���ʽΪ��3Pb+8H++2NO3=3Pb2++2NO��+4H2O��
(3)Pb��PbO��PbCO3�������������ת����Pb(NO3)2��Pb(NO3)2�м�ϡH2SO4ת����PbSO4�����ᣬHNO3��ѭ�����ã�������ܳ�Ǧ�����Һ��c(Pb2+)=1.82��105mol/L����֪Ksp(PbSO4)=1.82��108�����ʱc(SO42)=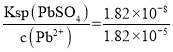 mol/L=1.00��103mol/L��
mol/L=1.00��103mol/L��
(4) �����̿�������Ǧ���������Ʒ�Ӧ�������λ�����Ǧ�������ƣ���Ӧ����ʽΪ��4PbSO4+6NaOH![]() 3PbOPbSO4H2O+3Na2SO4+2H2O��
3PbOPbSO4H2O+3Na2SO4+2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ӷ�Ǧ�����ص����ࣨ��Ҫ�ɷ�ΪPbSO4��PbO2������Ǧ��RSR ���յ���Ҫ�������£�
![]()
��1��Ǧ�����طŵ�ʱ�ܷ�ӦΪ��
Pb(s) �� PbO2(s) �� 2H2SO4(aq) �� 2PbSO4(s) �� 2H2O(l)
������Ӧ��PbO2(s) �� SO42��(aq) �� 4H+(aq) �� 2e�� �� PbSO4(s) �� 2H2O(l)
������Ӧ��________��
��2���������м���Na2CO3��Һ��PbSO4ת��Ϊ�����ܵ�PbCO3��
���û�ѧƽ���ƶ�ԭ��������ԭ��________��
�ڹ�ҵ�ϳ���NaHCO3��Һ����Na2CO3��Һ����PbSO4ת��ΪPbCO3��PbSO4��NaHCO3��Һ��Na2CO3��Һ��ͬ���ʵ�����ʱ��PbSO4��ת���ʼ��±���
�� | n(PbSO4)�� n(NaHCO3) | 1��1.5 | 1��2 | 1��3 |
PbSO4ת����/% | 95.5 | 96.9 | 97.8 | |
�� | n(PbSO4)�� n(Na2CO3) | 1��1.5 | 1��2 | 1��3 |
PbSO4ת����/% | 98 | 98 | 98 |
�����ϱ����ݣ����ʵ�������ͬʱ������PbSO4��ת���ʱȢ��е��Դ�ԭ����________��
��������Ӧ������PbCO3�⣬���������ɼ�ʽ̼��Ǧ[2PbCO3��Pb(OH)2]���������ȶ��ֽ�����PbO��ͨ��ʵ��ȷ�������к���2PbCO3��Pb(OH)2�����ʵ�������������________��ͨ������ʵ��ȷ��������2PbCO3��Pb(OH)2�ĺ���������ⶨ��������________��
��3�������м���Na2SO3��Һ��������������________��
��4��H2SiF4��Һ�ܽ�PbCO3�Ļ�ѧ����ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£������������ǿ��淴ӦA(g)+3B(g)![]() 2C(g)�ﵽƽ���־����( )
2C(g)�ﵽƽ���־����( )
��C������������C�ķֽ�������� ����λʱ����a mol A���ɣ�ͬʱ���� 3amolB ��A��B��C��Ũ�Ȳ��ٱ仯 ������������ѹǿ���ٱ仯 �������������ʵ������ٱ仯 ����λʱ������ a mol A��ͬʱ����3a mol B ��A��B��C�ķ�����Ŀ��Ϊ1:3:2
A.�ڢܢ�B.�ڢ�C.�٢ۢ�D.�ݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȳ�����![]() ��һ����Ҫ���л�����ԭ�ϣ��е�Ϊ103~105�档ʵ�����Ʊ�������Ȳ������ķ�ӦΪ��
��һ����Ҫ���л�����ԭ�ϣ��е�Ϊ103~105�档ʵ�����Ʊ�������Ȳ������ķ�ӦΪ��![]()
![]()
![]() ��װ������ͼ��
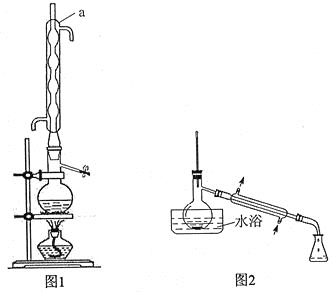
��װ������ͼ��
ʵ�鲽�����£�
����1���ڷ�Ӧƿ�У�����14.0g��Ȳ�ᡢ50ml�״���2mlŨ���ᣬ�������Ƭ������һ��ʱ��(װ�ü�ͼ1)��
����2�����������ļ״�(װ�ü�ͼ2)��
����3����ӦҺ��ȴ�������ñ���NaCl��Һ��5%Na2CO3��Һ��ˮϴ�ӡ�������л��ࡣ
����4���л��ྭ��ˮNa2SO4������ˡ����Ƶñ�Ȳ�����12.5g��
��1��װ��ͼ������a��������____________����������__________________��
��2��������ƿ�м������Ƭ��Ŀ����____________�������Ⱥ���δ�����Ƭ��Ӧ��ȡ����ȷ������____________________________��
��3������1�У���������״���Ŀ�ij����ܼ��⣬����________________��
��4������3�У���5%Na2CO3��Һϴ�ӣ���Ҫ��ȥ��������________________��������л���IJ�������Ϊ____________��
��5������4�У�����ʱ������ˮԡ���ȵ�ԭ����______________________________��
��6����ʵ��IJ�����________(����3λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ���ҷ�Һ��![]() ��Na+��Fe3+��Cr3+��
��Na+��Fe3+��Cr3+��![]() ��
��![]() �����ӣ���ͨ���������̱��Ϊ���Ʊ�K2Cr2O7��
�����ӣ���ͨ���������̱��Ϊ���Ʊ�K2Cr2O7��
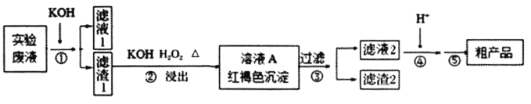
��֪��
(a)![]() ��
��![]()
(b)����������������������pH�������
�������� | pH | |
��ʼ���� | ��ȫ���� | |
Fe3+ | 2.7 | 3.7 |
Cr3+ | 4.9 | 6.8 |
��ش�
(1)ijͬѧ����ֽ�������жϲ���ټ���KOH�����Ƿ���ʡ��ڼ���һ����KOH��Һ����ëϸ��ȡ��������������ɫ��չ������Ѭ��İߵ���ͼ��ʾ������KOH���ʺϵ�ʵ������(ʵ��˳���Ѵ���)________��C�İߵ���ɫΪ________��
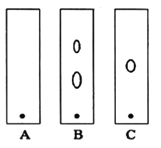
(2)����ں�Cr���ʷ�������Ҫ��Ӧ�����ӷ���ʽΪ________________________��
(3)������װ���У���Ӧѡ��________��(����)
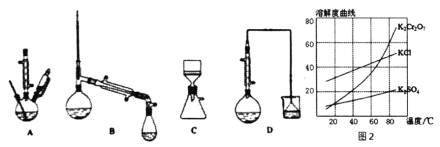
(4)�������ʵ��ܽ��������ͼ2������ݿ����õ����в��ֲ�����a�����������ִ������壬ֹͣ���ȣ�b����ȴ�����£�c����������Һ���־�Ĥ��ֹͣ���ȣ�d��ϴ�ӣ�e�����ȹ��ˣ�f�����ˡ���ѡ����ʲ�������ȷ˳��________��
(5)������к��ʵ�ϴ�Ӽ���________(����ˮ�Ҵ��������Ҵ�-ˮ���Һ��������ˮ��������ˮ��)��
(6)ȡmg�ֲ�Ʒ���250mL��Һ��ȡ25.00mL����ƿ�У���cmol��L-1��(NH4)2Fe(SO4)2����Һ�ζ�(���ʲ���Ӧ)�����ı�(NH4)2Fe(SO4)2��ҺVmL����ôֲ�Ʒ��K2Cr2O7�Ĵ���Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������д��ȷ����
A.![]()
![]() ������ͬ�����£�
������ͬ�����£�![]() �������������1mol������1mol����������֮��
�������������1mol������1mol����������֮��
B.![]()
![]() ����Ӧ����ܼ���С����������ܼ���
����Ӧ����ܼ���С����������ܼ���
C.��![]() ��ϡ��Һ��ϡ������ȫ�кͣ��ų�
��ϡ��Һ��ϡ������ȫ�кͣ��ų�![]() �����������ʾ���кͷ�Ӧ���Ȼ�ѧ����ʽΪ
�����������ʾ���кͷ�Ӧ���Ȼ�ѧ����ʽΪ![]()
![]()
D.![]() ��30MPaʱ��������Ӧ
��30MPaʱ��������Ӧ![]()
![]()
![]() �ڴ������½�
�ڴ������½�![]() ����
����![]() ��ַ�Ӧ���ų�����
��ַ�Ӧ���ų�����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����е�������18O����������Ҵ���һ�������·�Ӧ�������㹻����ʱ�����ϵ�к���18O��������
A. ֻ������
B. ֻ����������
C. ���ᡢ����������ˮ
D. �����������Ҵ���ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ0.1molNa2CO3���������������Ϊ1L����Һ�в���������ҺpHֵ֮���ϵ��ͼ��ʾ������������ȷ����
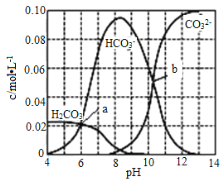
A.���Һ��pH����![]() ��������С
��������С
B.b��ʱ��Һ�����Ӵ������¹�ϵ��2c(![]() )+c(
)+c(![]() )+c(OH-)=c(Na+)+c(H+)
)+c(OH-)=c(Na+)+c(H+)
C.H2CO3��һ�����볣��Ka1ԼΪ10-6,Ka2��������Ϊ10-11
D.pH=7ʱ����Һ������Ũ�ȴ�С˳��Ϊ:c(Na+)=c(Cl-)>c(![]() )>c(H+)=c(OH-)>c(
)>c(H+)=c(OH-)>c(![]() )
)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com