
【题目】下面图(1)和图(2)是A、B两种物质的核磁共振氢谱。已知A、B两种物质都是烃类,都含有6个氢原子。请根据图(1)和图(2)两种物质的核磁共振氢谱图选择出可能属于图(1)和图(2)的两种物质 ( )

A. A是C3H8;B是C6H6 B. A是C4H10;B是C6H6
C. A是C3H6;B是C3H6 D. A是C3H6;B是C2H6
【答案】C
【解析】由图(1)可得:A物质只有一种环境的氢;由图(2)可得:B物质有三种环境的氢,氢原子个数比大约是3:2:1。A项,C3H8一定是丙烷,分子中有两种环境的氢,一定不是A,也不是B,故A项错误。B项,C4H10可能为正丁烷或异丁烷,都有两种环境的氢,既不是A也不是B,故B项错误。C项,C3H6可能是丙烯,也可能是环烷烃,如果是丙烯,则有三种环境的氢,氢原子个数比是3:2:1;如果是环烷烃,分子中只有一种环境的氢,综合这2种情况可得:C3H6可能是A,也可能是B,故C项正确。D项,C2H6只能是乙烷,分子中只有一种环境的氢,可能是A物质,一定不是B物质,故D项错误。综上,选C。


科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量共存的是 ( )
A. 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
B. 在强碱性溶液中:Na+、K+、Al(OH)4-、CO32-
C. 在碱性溶液中:NH4+、Al3+、SO42-、NO3-
D. 常温下在pH=1的溶液中:K+、Fe2+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素在生物体内含量虽很少,却是维持正常生命活动不可缺少的。下列实例 可证实该理论的是( )
A. 缺Mg 叶片变黄
B. 油菜缺B时只开花不结果
C. 动物血液中钙盐的含量太低会抽搐
D. 缺P会影响ATP的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的量的说法中,正确的是
A. Mg的摩尔质量为24 g
B. 物质的量的单位是摩尔
C. 1 mol O2在任何条件下的体积都为22.4 L
D. 将1 mol NaCl晶体加入到1L水中,得到NaCl溶液的浓度就是1 mol L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧的烟气中含有SO2和NO,直接排放会形成酸雨、污染大气,因此对烟气进行脱硫、脱硝具有重要意义。
(1)选择性催化还原技术是目前成熟的烟气脱硝技术,即在金属催化剂作用下,用还原剂(如NH3)选择性地与NO反应生成N2和H2O。
①已知:4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g) ΔH = -905.5kJ/mol
4NO(g) + 6H2O(g) ΔH = -905.5kJ/mol
N2(g) + O2(g) ![]() 2NO(g) ΔH =+180 kJ/mol
2NO(g) ΔH =+180 kJ/mol
则该方法中主要反应的热化学方程式是(请补充完整):
4NH3(g) + 4NO(g) + O2(g)![]() 4N2(g) + 6H2O(g) ΔH =_________
4N2(g) + 6H2O(g) ΔH =_________
②该方法控制反应温度在315~400℃之间,反应不宜过低也不能过高的原因是_________。
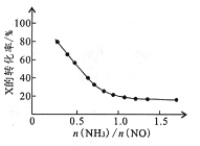
③氨氮比[n(NH3)/n(NO)]的大小会影响该方法的脱硝率。350℃时,只改变NH3的投放量,反应物X的转化率与氨氮比的关系如右图,则X是_____(填化学式)。氨氮比由0.5增加到1.0时,脱硝主要反应的平衡将向____________方向移动。当氨氮比大于1.0时,烟气中NO浓度反而增大,主要原因是___________。
(2)将烟气中的SO2、NO经O3处理后,再用CaSO3悬浊液吸收,可脱硫、脱硝。
已知:O3氧化烟气中SO2、NO的主要反应为:
NO + O3![]() NO2 + O2; 2NO + O2
NO2 + O2; 2NO + O2![]() 2NO2; SO2+ O3
2NO2; SO2+ O3![]() SO3 + O2
SO3 + O2
用CaSO3悬浊液(pH=8)吸收经O3处理后的烟气时,NO2转化为NO2-,离子方程式为
_____________。
② 在CaSO3悬浊液中加入Na2SO4溶液可提高NO2的吸收速率,请结合化学原理进行解释___________________________。
③烟气经处理后最终得到含Na+、NO2-、SO42-的吸收液。t℃时,向吸收液中加入AgNO3溶液至SO42-恰好完全沉淀(即SO42-浓度等于1.0×10-5 mol·L-1)时,c(NO2-)=_______mol/L。[t℃时,AgNO2(亚硝酸银)的 Ksp= 9.0×10-4、Ag2SO4的Ksp=4.0×10-5。]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进入20世纪以后,化学科学经历了迅速发展的“创新百年”。下列各项中,不属于这个时期的化学重大成就的是
A. 制陶技术的成熟应用 B. 现代量子化学理论的建立
C. 化学工业的迅速发展 D. 放射性元素的发现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3,5-二甲氧基苯酚是重要的有机合成中间体,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
甲醇 | 64. 7 |
| 0. 7915 | 易溶于水 |
乙醚 | 34. 5 |
| 0. 7138 | 微溶于水 |
3,5-二甲氧基苯酚 |
| 33 ~36 |
| 易溶于甲醇、乙醚,微溶于水 |
(1)1mol间苯三酚完全燃烧需要______molO2。
(2)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是的__________。
②萃取用到的分液漏斗使用前需____________并洗净,分液时有机层在分液漏斗的______填(“上”或“下”)层。
(3)分离得到的有机层依次用饱和NaHCO3溶液、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是_________________________________________ ;
(4)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_____________(填字母)。
a.蒸馏除去乙醚 b.冷却结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(5)反应可能出现的副产物的结构简式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国药学家屠呦呦因发现青蒿素治疗疟疾新方法而获得2015年诺贝尔生理学奖。这是中国本土培养的科学家首次获得诺贝尔奖。请回答下列有关问题:
(1)青蒿素的分子式为C15H22O5,其组成中的三种元素的电负性有大大小排序是_______,其中第一电离能最大元素基态原子的核外电子排布式为______________。
(2)在确定青蒿素结构的过程中,可采用KBH4作为还原剂,其制备流程如下:

①已知金属晶体Na的配位数为8,则其晶胞结构图符合图1的_____________(选填字母编号),其堆积方式为_______(填名称)

②图2是NaH的晶胞结构,则NaH晶胞中Na+的数目为_________,若该晶体密度为ρg·cm-3,则晶胞中相距最近的两个Na+间的距离为________cm(用含ρ、NA的代数式表示)。
③化合物B(OCH3)3中C的杂化轨道类型为________,B(OCH3)3的空间构型为________,与其具有相同空间构型的分子和离子有________、_________(分子或离职各写一种)。
④KBH4的电子式__________,晶体结构中存在的作用力有______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com