
| A、单质 | B、化合物 |
| C、混合物 | D、氧化物 |
 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
| A、平衡时NO2的体积分数:甲>乙 |
| B、达到平衡所需要时间,甲比乙多 |
| C、平衡时的颜色,甲比乙深 |
| D、平衡时的平均相对分子质量:甲<乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、75% | B、25% |
| C、50% | D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
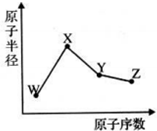 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强,下列说法正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强,下列说法正确的是( )| A、对应气态氢化物的稳定性Y>Z |
| B、化合物XZW既含离子键也含共价键 |
| C、对应简单离子半径W<X |
| D、Y的氧化物能与Z或X的最高价氧化物对应的水化物反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单质:水银、石墨、氦气、HD |
| B、氧化物:金刚砂、Na2O2、双氧水、N2O4 |
| C、混合物:水玻璃、盐酸、胆矾、AgI胶体 |
| D、盐:碱式碳酸铜、小苏打、KI,Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | Si-Si键 | H-H键 | Cl-Cl键 | H-Cl键 | Si-Cl键 |
| 键能(KJ/mol) | 176 | 436 | 243 | 431 | 360 |
查看答案和解析>>
科目:高中化学 来源: 题型:
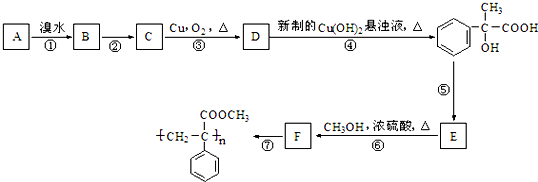
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com