
| A��CuS��Cu(OH)2��CuCO3 | B��CuCO3��Cu(OH)2����uS |
| C��CuS��CuCO3��Cu(OH)2 | D��Cu(OH)2����uCO3��CuS |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| | CH3COOAg | AgCl | Ag2CrO4 | Ag2S |
| Ksp | 2.3��10��3 | 1.77��10��10 | 1.12��10��12 | 6.7��10��15 |
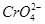 ��Cl������Һ����������AgNO3��Һʱ��
��Cl������Һ����������AgNO3��Һʱ��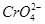 �ȳ���
�ȳ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
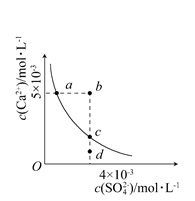
| A�����κ���Һ�У�c(Ca2��)��c(SO42��)����� |
| B��b�㽫�г������ɣ�ƽ�����Һ��c(SO42��)һ������3��10��3mol��L��1 |
| C��a���Ӧ��Ksp����c���Ӧ��Ksp |
| D��d����Һͨ���������Ա䵽c�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
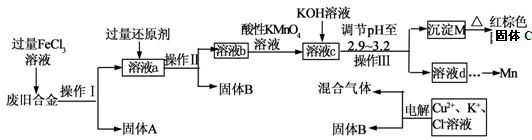
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��MgCO3��CaCO3��MnCO3��KSP�������� |
| B��a��ɱ�ʾ MnCO3�ı�����Һ����c��Mn2+��=c��CO32���� |
| C��b��ɱ�ʾCaCO3�ı�����Һ����c��Ca2+��<c��CO32���� |
| D��c��ɱ�ʾMgCO3�IJ�������Һ����c��Mg2+��>c��CO32���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
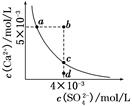
| A�����κ���Һ�У�c(Ca2��)��c(SO42-)����� |
| B��b�㽫�г������ɣ�ƽ�����Һ��c(SO42-)һ������3��10��3 mol/L |
| C��a���Ӧ��Ksp����c���Ӧ��Ksp |
| D��d����Һͨ���������Ա䵽c�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ���� | AgCl | AgI | Ag2S |
| ��ɫ | �� | �� | �� |
| Ksp(25 ��) | 1.8��10-10 | 1.5��10-16 | 1.8��10-50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Ag+��aq�� + Cl-��aq����ƽ��ʱ��Ksp =C��Ag+ )��C(Cl-) ,�����Ȼ����ֱ�Ͷ���100 mLˮ ��24 mL 0��1 mol��L-1NaCl ��10 mL 0��1 mol��L-1MgCl2 ��30 mL 0��1 mol��L-1AgNO3��Һ��,��Һ��C(Ag+)�ɴ�С˳��Ϊ
Ag+��aq�� + Cl-��aq����ƽ��ʱ��Ksp =C��Ag+ )��C(Cl-) ,�����Ȼ����ֱ�Ͷ���100 mLˮ ��24 mL 0��1 mol��L-1NaCl ��10 mL 0��1 mol��L-1MgCl2 ��30 mL 0��1 mol��L-1AgNO3��Һ��,��Һ��C(Ag+)�ɴ�С˳��Ϊ | A���ۢ٢ڢ� | B���ܢ٢ڢ� | C���٢ڢۢ� | D���ܢۢڢ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com