
【题目】下列电离方程式正确的是( )
A.CuCl2═Cu2++Cl2﹣
B.Al2(SO4)3=2Al3++3SO ![]()
C.Fe2(SO4)3═2Fe2++3SO ![]()
D.Ba(NO3)2═Ba2++2(NO3)2﹣
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】据《科学快递》报道,研究人员拍摄到化学键形成过程中的过渡状态。化学键不存在于( )
A.原子与原子之间B.分子与分子之间
C.离子与离子之间D.离子与电子之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中的少量杂质(括号内的物质为杂质),所选用的试剂或方法不正确的是( )
A.CO2(SO2):饱和酸性KMnO4溶液
B.Cl2(HCl):饱和NaCl溶液
C.CO2(乙烯):通入溴的CCl4溶液
D.乙酸乙酯(乙酸):氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是500 ℃时, 1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图。若在温度恒定,体积不变的容器中反应达到平衡,再充入NO2则,ΔH________(填“增大”、“减小”或“不变”,下同)。请写出NO2和CO反应的热化学方程式:__________。该反应能自发进行的主要原因为_____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用右图表示的一些物质或概念间的从属关系中不正确的是( )
X | Y | Z | |
A | 氧化物 | 化合物 | 纯净物 |
B | 胶体 | 分散系 | 混合物 |
C | 含氧酸 | 一元酸 | 酸 |
D | 碱性氧化物 | 金属氧化物 | 氧化物 |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修3:物质结构与性质】
2015年我国自主研制的C919大型客机正式下线,标志着我国成为世界上少数几个掌握研发制造大型客机能力的国家,同时意味着中国高端装备制造业发展到一个全新的高度。
(1)飞机的外壳通常采用镁、铝、钛合金材料,钛的价电子排布图为__________,第一电离能:镁 _________铝(填“大于”或“小于”)。
(2)Fe与CO能形成配合物羰基铁[Fe(CO)5],该分子中σ键与π键个数比为________。
(3)SCl2分子中的中心原子杂化轨道类型是_______,该分子构型为_________。
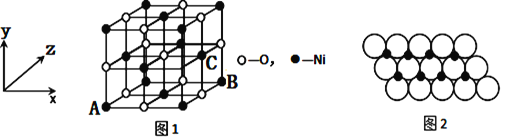
(4)已知MgO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69 pm。则熔点:MgO_____NiO(填“>”、“<”或“=”),理由是_____________。
(5)如图1所示,NiO晶胞中离子坐标参数A为(0,0,0),B为(1,0,1),则C离子坐标参数为___________。
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为a m,每平方米面积上分散的该晶体的质量为______g。(用a、NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关苯与乙烯的比较中,正确的是( )
A.分子中所有原子都在同一平面上
B.等质量燃烧时,苯耗氧多
C.都能与溴水反应
D.都能被酸性高锰酸钾溶液氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B、D、C、A、E五种元素的原子序数顺序依次增大,其中只有E为金属元素,D、C元素在元素周期表中位置相邻,在一定条件下,B的单质可以分别和A、C、D的单质化合生成甲、乙、丙化合物,C的单质和D的单质化合可得丁,戊、己、庚均为化合物。已知乙、丙每个分子中均含有10个电子,下图为相互转化关系:
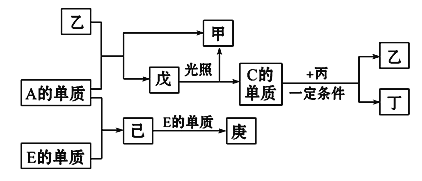
请回答下列问题:
(1)写出E的原子结构示意图_________________________。
(2)写出C、D氢化物的稳定性由强到弱的顺序____________。(用化学式表示)。
(3)A、B、D三种元素形成的化合物中,含有化学键的类型为___________。
(4)写出C与丙反应的化学反应方程式_________________________________。
(5)写出工业上从海水中制取A的离子反应方程式____________________________。
(6)工业上通过如下转化可制得含A元素的钾盐KAO3晶体:

①完成Ⅰ中反应的总化学方程式: ________
NaA+ H2O![]() NaAO3+
NaAO3+
②Ⅱ中反应过程能析出KClO3晶体而无其他晶体析出的原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g·100 mL-1)。
Ⅰ.实验步骤:
(1)配制待测白醋溶液。用________________(填仪器名称)量取10.00 mL食用白醋,在__________(填仪器名称)中用水稀释后转移到100 mL__________(填仪器名称)中定容,摇匀即得待测白醋溶液。
(2)量取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴酚酞作指示剂。
(3)读取盛装0.100 0 mol·L-1NaOH 溶液的碱式滴定管的初始读数。
(4)滴定。判断滴定终点的现象是:_________________,到达滴定终点,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
(5)如图是某次滴定时的滴定管中的液面,其读数为________mL。
![]()
Ⅱ.实验记录
实验数据(mL) 滴定次数 | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论:
(1)甲同学在处理数据时计算得:平均消耗的NaOH溶液的体积V= mL=15.24 mL。指出他计算的不合理之处:______。按正确数据处理,得c(市售白醋)=_____mol·L-1;市售白醋总酸量=_____g·100 mL-1。
mL=15.24 mL。指出他计算的不合理之处:______。按正确数据处理,得c(市售白醋)=_____mol·L-1;市售白醋总酸量=_____g·100 mL-1。
(2)乙同学仔细研究了该品牌白醋的标签,发现其中还含有苯甲酸钠作为食品添加剂,他想用资料法验证醋酸与苯甲酸钠不会发生复分解反应,需查找在一定温度下的________(填序号)。
A.pH B.电离度 C.电离平衡常数 D.溶解度
(3)在本实验的滴定过程中,下列操作会使实验结果偏大的是_________(填写序号)。
A.碱式滴定管在滴定时未用标准NaOH溶液润洗
B.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
C.锥形瓶中加入待测白醋溶液后,再加少量水
D.锥形瓶在滴定时剧烈摇动,有少量液体溅出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com