
常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
| 实验编号 | c(HA)/mol·L-1 | c(NaOH)/mol·L-1 | 混合溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.2 | 0.2 | pH=9 |
| 丙 | c1 | 0.2 | pH=7 |
| 丁 | 0.2 | 0.1 | pH<7 |
科目:高中化学 来源: 题型:单选题
室温下,将0.100 0 mol·L-1盐酸滴入20.00 mL 未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体 积变化曲线如图所示。下列有关说法不正确的是( )
| A.b点:c(M+)+c(MOH)=c(Clˉ) |
| B.a到b点的水溶液导电性依次增强 |
| C.该一元碱溶液浓度为0.100 0 mol·L-1 |
| D.室温下,MOH的电离常数Kb=1×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
H2S水溶液中存在电离平衡H2S H++HS-和HS-
H++HS-和HS- H++S2-。若向H2S溶液中
H++S2-。若向H2S溶液中
| A.滴加新制氯水,溶液pH减小 | B.通入过量SO2气体,溶液pH增大 |
| C.加水,溶液中氢离子浓度增大 | D.加入少量硫酸铜固体,所有离子浓度都减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25℃时,有c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是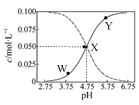
| A.Y点所表示的溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) |
| B.W点所表示的溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol·L-1 |
| C.该温度下醋酸的电离平衡常数为10—4.75 mol·L-1 |
| D.向X点所表示的溶液中加入等体积的0.05 mol·L-1 NaOH溶液 :c(H+)=c(CH3COOH)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列与含氯化合物有关的说法正确的是
| A.HClO是弱酸,所以NaClO是弱电解质 |
| B.向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 |
| C.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 |
| D.电解NaCl溶液得到22.4 L H2(标准状况),理论上需要转移NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
A pH=4的醋酸中:c(H+)=4.0molL-1
B 饱和小苏打溶液中:c(Na+)= c(HCO3-)
C 饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-)
D pH=12的纯碱溶液中:c(OH-)=1.0×10-2molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,pH=11的氨水溶液和pH=1的盐酸溶液等体积混合后(不考虑混合后溶液体积的变化),恰好完全反应,则下列说法不正确的是( )
| A.弱碱的浓度大于强酸的浓度 |
| B.反应完全后的溶液呈碱性 |
| C.原氨水中有1%的含氮微粒为NH4+ |
| D.反应后的溶液中NH4+、NH3·H2O与NH3三种微粒的平衡浓度之和为0.05 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,0.1 mol·L-1某一元酸HA溶液中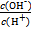 =1×10-12,下列说法中正确的是
=1×10-12,下列说法中正确的是
| A.溶液中由水电离出的c(H+)=1×10-10 mol·L-1 |
B.溶液中存在HA H++A- H++A- |
| C.与0.1 mol·L-1 NaOH溶液等体积混合后所得溶液为中性 |
| D.原溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知298 K时下列物质的溶度积(单位略)。
| | CH3COOAg | AgCl | Ag2CrO4 | Ag2S |
| Ksp | 2.3×10-3 | 1.77×10-10 | 1.12×10-12 | 6.7×10-15 |
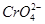 和Cl-的溶液中慢慢滴入AgNO3溶液时,
和Cl-的溶液中慢慢滴入AgNO3溶液时,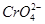 先沉淀
先沉淀查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com