
【题目】屠呦呦率领的研究团队最初采用水煎的方法提取青蒿素,实验证明水煎剂对治疗疟疾无效,研究发现这是因为青蒿素分子中的某个基团对热不稳定,该基团还能与碘化钠作用生成碘单质。进一步研究发现,通过如下所示反应制得的双氢青蒿素比青蒿素水溶性好,所以治疗疟疾的效果更好。

下列推测不正确的是
A. 低温、有机溶剂冷浸可能是提取青蒿素的有效方法
B. 质谱或核磁共振氢谱都可以鉴别青蒿素和双氢青蒿素
C. 影响青蒿素治疗疟疾的药效的主要官能团是—O—O—
D. 双氢青蒿素比青蒿素水溶性好的原因为O—H是极性键而C=O是非极性键
【答案】D
【解析】
A. 过氧键对热不稳定,高温时易断裂;
B. 青蒿素和双氢青蒿素的相对分子质量与氢原子所处的环境均不同;
C. 水煎剂破坏了过氧键,导致治疗疟疾无效;
D. C=O是极性键,有机物分子含羟基越多,越易溶于水。
A. 过氧键对热不稳定,高温时易断裂,则低温、有机溶剂冷浸可以减少药物提取过程中过氧键的断裂,故A项正确;
B. 根据图示信息可知,青蒿素与氢气发生加成反应生成双氢青蒿素后,其相对分子质量与等效氢化学环境的种类不同,故可用质谱或核磁共振氢谱鉴别青蒿素和双氢青蒿素,故B项正确;
C. 根据题设信息可知,影响青蒿素治疗疟疾的药效的主要官能团是过氧键—O—O—,过氧键对热不稳定,水煎的方法对治疗疟疾无效,故C项正确;
D. 根据相似相容原理可知,青蒿素分子内的酯基(![]() 是极性键)不如双氢青蒿素分子内的羟基易溶于水,则双氢青蒿素比青蒿素水溶性好,故D项错误;
是极性键)不如双氢青蒿素分子内的羟基易溶于水,则双氢青蒿素比青蒿素水溶性好,故D项错误;
答案选D。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】 N2(g)与H2(g)在铁催化剂表面经历如下过程生成NH3(g),则下列说法正确的是

A.Ⅰ中破坏的均为极性键
B.Ⅳ中NH2与H2生成NH3
C.Ⅱ、Ⅲ、Ⅳ均为放热过程
D.N2(g)+3H2(g)![]() 2NH3(g)1mol氮气完全反应放热44kJ
2NH3(g)1mol氮气完全反应放热44kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R 皆为前20号元素,其原子半径与化合价的关系如图所示。下列说法错误的是

A.QX 中只存在离子键
B.简单离子半径:r(M-)>r(Q+)>r(R2+)
C.X、Y、Z 三种元素组成的化合物可能是盐或碱
D.ZM3 各原子最外层电子数均满足8 电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中的一些常见物质有如图转化关系。其中A、H为空气中的主要成分,气体B能使湿润的红色石蕊试纸变蓝,气体D遇到A很快变成红棕色E,C属于氧化物,I是紫红色金属单质。X为常见液体(部分反应条件及生成物没有全部列出)。

回答下列问题。
(1)C的化学式为________。
(2)X的电子式为________。
(3)写出反应①的化学方程式__________________________________________。
(4)写出反应②的离子方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从含碘废液(除H2O外,含有CCl4、I2、![]() 等)中回收碘,实验过程如下:
等)中回收碘,实验过程如下:

(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_______;该操作将I2还原为I-的目的是___________________。
(2)操作![]() 的名称为__________。
的名称为__________。
(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是__________________;仪器a的名称为________;仪器b中盛放的溶液为__________。

(4)已知:![]() ;某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
;某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
①取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在;
②_______________________________________________________________________________;
③另从水层中取少量溶液,加入1-2mL淀粉溶液,加盐酸酸化后,滴加Na2SO3溶液,若溶液变蓝说明废水中含有IO3-;否则说明废水中不含有IO3-。
(5)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂和水处理剂。现用ClO2氧化酸性含废液回收碘。完成ClO2氧化I-的离子方程式:________________________________。
(6)“碘量法”是一种测定S2-含量的有效方法。立德粉ZnS·BaSO4是一种常用的白色颜料,制备过程中会加入可溶性的BaS,现用“碘量法”来测定立德粉样品中S2-的含量。称取m g样品,置于碘量瓶中,移取25.00 mL 0.1000 mol/L 的I2-KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5min,有单质硫析出。以淀粉为指示剂,过量的I2用0.1000 mol/L Na2S2O3 滴定,反应式为I2 + 2S2O32-=2I-+ S4O62-。测定消耗Na2S2O3溶液体积V mL。立德粉样品S2-含量为__________(写出表达式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钾的冶炼可采用如下方法:2KF+CaC2![]() CaF2+2K↑+2C,下列有关说法合理的是( )
CaF2+2K↑+2C,下列有关说法合理的是( )
A.该反应的氧化剂是KF,氧化产物是K
B.该反应能说明C的还原性大于K
C.电解KF溶液不可能制备金属钾
D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含Fe(NO3)3、Cu(NO3)2、HNO3的某稀溶液,若向其中逐步加入铁粉,溶液中Fe2+浓度与加入铁粉的物质的量之间的关系如右图所示,则该溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为( )

A. 1∶1∶3B. 1∶2∶4C. 1∶1∶4D. 1∶3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列图象的说法正确的是( )
A. 表示的反应速率随温度变化的关系可知该反应的△H>0

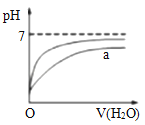
B. 表示向pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,则其中曲线a对应的是醋酸
C. 表示该反应为放热反应,且催化剂能降低反应的活化能、改变反应的焓变

D. 中开关K置于a或b处均可减缓铁的腐蚀

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. ![]() =1×10-12的溶液:Na+、K+、ClO-、CO32-
=1×10-12的溶液:Na+、K+、ClO-、CO32-
B. 滴入酚酞变红色的溶液:K+、Ca2+、HCO3-、CO32-
C. 能溶解Al(OH)3的溶液:K+、NH4+、NO3—、CH3COO—
D. 0.1mol/LFe(NO3)2溶液:H+、Cu2+、SO42—、Cl—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com