
【题目】中学化学中的一些常见物质有如图转化关系。其中A、H为空气中的主要成分,气体B能使湿润的红色石蕊试纸变蓝,气体D遇到A很快变成红棕色E,C属于氧化物,I是紫红色金属单质。X为常见液体(部分反应条件及生成物没有全部列出)。

回答下列问题。
(1)C的化学式为________。
(2)X的电子式为________。
(3)写出反应①的化学方程式__________________________________________。
(4)写出反应②的离子方程式__________________________________________。
【答案】CuO ![]() 4NH3+5O2
4NH3+5O2![]() 4NO+6H2O 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
4NO+6H2O 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
【解析】
A、H为空气中主要成分,分别为N2、O2中的一种,气体B能使湿润的红色石蕊试纸变蓝,则B为NH3,A能与氨气反应生成D与X,X为常见液体,气体D遇到A很快变成红棕色E,可推知A为O2,H为N2,D为NO,X为H2O,E为NO2,E与X反应生成F,I是紫红色金属单质,应为Cu,F与Cu反应得到G、X(水)、D(NO),故F为HNO3,G为Cu(NO3)2,C属于氧化物,与B(NH3)反应得到X(水)、H(氮气)、I(Cu),根据元素守恒可知C为CuO,据此解答。
根据上述分析可知A是O2,B是NH3,C是CuO,D是NO,E是NO2,F是HNO3,G是Cu(NO3)2,H是N2,I是Cu,X是H2O。
(1) 由上述分析可知C是氧化铜,化学式为CuO;
(2)X为H2O,两个H原子与1个O原子形成2对共用电子对,电子式为![]() ;(3)反应①是NH3的催化氧化反应,化学方程式为:4NH3+5O2
;(3)反应①是NH3的催化氧化反应,化学方程式为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(4)反应②是Cu与稀硝酸反应产生Cu(NO3)2、NO和水,根据电子守恒、电荷守恒、原子守恒,可得离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】(1)3.01×1024个OH的物质的量为________mol,含有电子的数目为________,这些OH和________gNa+含有的电子数相同。
(2)标准状况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为______;
(3)实验室为确定一瓶稀盐酸的浓度,用0.1000mol/LNaOH溶液中和25.00mL该盐酸,当酸与碱恰好完全反应时,消耗NaOH溶液24.50mL。该盐酸的物质的量浓度为______;
(4)实验室可以用高锰酸钾和浓盐酸反应制备氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,用双线桥标出电子转移的方向和数目___________,该反应中被氧化的元素是________,参加反应的氧化剂与还原剂的物质的量之比为________,如果该反应过程中转移了5mol电子,生成的氯气在标准状况下体积为__________L(假设气体全部逸出)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.某单烯烃与H2 加成后的产物为(C2H5)2CHCH2C(CH3)3,则该烯烃可能的结构简式有5种
B. 有机物的名称是2,4,4-三甲基戊烷
有机物的名称是2,4,4-三甲基戊烷
C.甲苯与氯气在光照下反应主要生成2,4,6-三氯甲苯
D.沼气、油田气和可燃冰中均含有甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向200 mL FeBr2溶液中逐渐通入Cl2,其中n(Fe 3+)、n(Br2) 随通入n(Cl2)的变化如图所示,下列说法不正确的是( )

A.氧化性强弱:Br2 > Fe3+
B.由图可知,该FeBr2溶液的浓度为1 mol·L-l
C.n(Cl2)=0. 12 mol时,溶液中的离子浓度有c (Fe 3+)∶c( Br-)=1∶8
D.n(FeBr2)∶n(Cl2)=1∶1时,反应的离子方程式为:2Fe2++2Br- + 2Cl2=2Fe3++Br2 + 4Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X中仅可能含有K+、Na+、Fe2+、Fe3+、NH4+、SO42-、SO32-、CO32-、I-、Cl-中的一种或多种,且溶液中各离子浓度相同。现进行下列实验,下列说法正确的是 ( )

A.该溶液X中可能有Fe3+、Na+
B.该溶液可能由是硫酸亚铁、碘化钾和氯化铵溶于水后得到的
C.如果气体Y能使湿润的蓝色石蕊试纸变红,说明溶液中一定含有NH4+
D.取样溶液Z,滴加氯化钡溶液出现沉淀,可推出X中一定存在SO42-、SO32-中的某一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钇的常见化合价为+3价,我国蕴藏着丰富的含钇矿石(Y2FeBe2Si2O10),工业上通过如下生产流程可获得氧化钇。
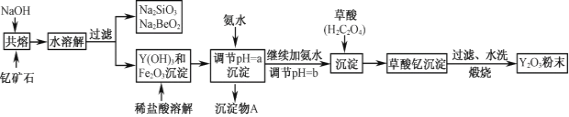
已知:①该流程中有关金属离子形成氢氧化物沉淀时的pH见下表:
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe3+ | 2.1 | 3.1 |
Y3+ | 6.0 | 8.2 |
②在元素周期表中,铍元素和铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)写出Na2SiO3的一种用途________________________。
(2)若改用氧化物的形式表示Y2FeBe2Si2O10组成,则化学式为__________。
(3)根据元素周期表的知识判断,常温下,氯化锶溶液pH____7(填“大于”、“等于”或“小于”);写出氯化锶的电子式:______________________。
(4)欲从Na2SiO3和Na2BeO2混合溶液中制得Be(OH)2沉淀。
① 最好选用盐酸和_______两种试剂,再通过必要的操作即可实现。
A.NaOH溶液 B.氨水 C.CO2 D.HNO3
② 写出Na2BeO2与足量盐酸发生反应的离子方程式___________________________。
(5)为使Fe3+沉淀完全,用氨水调节pH=a时,a应控制在_________范围内;继续加氨水调节pH =b发生反应的离子方程式为____________________________;检验Fe3+是否沉淀完全的操作方法是:___________________________________。
(6)煅烧草酸钇时发生分解反应,其固体产物为氧化钇,气体产物能使澄清石灰水变浑浊。写出草酸钇[Y2(C2O4)3·nH2O]煅烧的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】屠呦呦率领的研究团队最初采用水煎的方法提取青蒿素,实验证明水煎剂对治疗疟疾无效,研究发现这是因为青蒿素分子中的某个基团对热不稳定,该基团还能与碘化钠作用生成碘单质。进一步研究发现,通过如下所示反应制得的双氢青蒿素比青蒿素水溶性好,所以治疗疟疾的效果更好。

下列推测不正确的是
A. 低温、有机溶剂冷浸可能是提取青蒿素的有效方法
B. 质谱或核磁共振氢谱都可以鉴别青蒿素和双氢青蒿素
C. 影响青蒿素治疗疟疾的药效的主要官能团是—O—O—
D. 双氢青蒿素比青蒿素水溶性好的原因为O—H是极性键而C=O是非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于下列实验现象的解释,不合理的是
实验 | 现象 | 解释 | |
A | | ②中产生气体的速率比①慢 | 乙醇分子中,乙基对羟基产生影响,使O—H键不容易断裂 |
B |
| ③中振荡静置后分层,上层为橙色;④中产生白色沉淀 | 苯酚分子中,苯环对羟基产生影响,使O—H键更容易被取代 |
C |
| ⑤中振荡静置后分层,下层为紫色溶液;⑥中振荡后紫色溶液褪色 | 甲苯分子中,苯环对甲基产生影响,使甲基上C—H更容易被氧化 |
D |
| 水浴加热,⑦中未见明显变化;⑧中试管壁上附着一层光亮的银 | 碱性条件下+1价的Ag才能氧化乙醛 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是前四周期除稀有气体之外原子序数依次增大的七种元素。A与其他元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题:
(1)写出元素名称:B_______,G_______。
(2)写出F的价电子排布图:_______。
(3)写出化合物BC的结构式:__________________。
(4)由A、C、F三元素形成的离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是________________。
(5)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是______________________。
(6)E的一种晶体结构如图甲,则其一个晶胞中含有_______个E;G与D形成的化合物的晶胞结构如图乙,若晶体密度为ag/cm3,则G与D最近的距离为____pm
(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com