
| A.陶瓷是一种应用广泛的普通硅酸盐材料 |
| B.实验过程中产生的NO2尾气可以用NaOH溶液吸收 |
| C.实验室可用浓硫酸干燥氨气 |
| D.误服重金属盐造成的中毒可服用牛奶解毒 |
科目:高中化学 来源:不详 题型:单选题
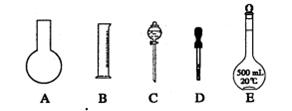
| A.用水吸收氨气时的导气管 |
| B.石油分馏时测量温度所用的温度汁 |
| C.用乙醇制备乙烯时所用的温度计 |
| D.用NaOH溶液和Fe2(SO4)3溶液制备Fe(OH)3、时,吸有NaOH溶液的胶头滴管 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
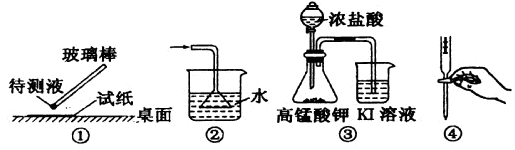
| A.①用pH试纸测某溶液的酸碱性 | B.②吸收氨气制氨水 |
| C.③探究氧化性:KMnO4>Cl2>I2 | D.④中和滴定实验 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
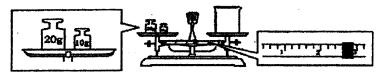
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在“食醋总酸含量的测定”实验中,选择酚酞溶液为指示剂,当溶液的颜色变为粉红色且在半分钟内不褪色,即达到滴定终点 |
| B.在“牙膏中某些主要成分的检验”实验中,在牙膏与蒸馏水搅拌、静置分离后的澄清溶液中加入少量的新制Cu(OH)2,当产生绛蓝色沉淀时,说明牙膏中含有甘油 |
| C.在“阿司匹林的合成”实验中,把从盐酸中析出的晶体进行抽滤,用酒精洗涤晶体1~2次,然后抽滤,将晶体转移到表面皿上,干燥后称其质量,计算产率。 |
| D.人体吸入氯气、氯化氢气体时,可吸入少量酒精或乙醚的混合蒸气解毒;氨气、溴中毒休克时要马上进行人工呼吸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
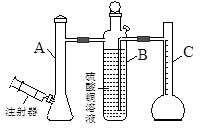
| A.反应前后抽气使B中导管内外液面持平 |
| B.用饱和食盐水代替A装置中的蒸馏水 |
| C.把A装置浸入盛有冰水混合物的水槽中 |
| D.在B装置中的硫酸铜溶液表面覆盖一层苯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
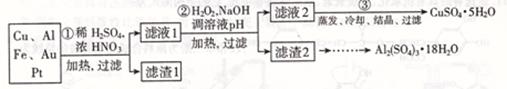
| 沉淀物 | Fe( OH)2 | Fe( OH)3 | Al( OH)3 | Cu( OH)2 |
| 开始沉淀 | 5.8 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 8.8 | 3.2 | 5.2 | 6.7 |
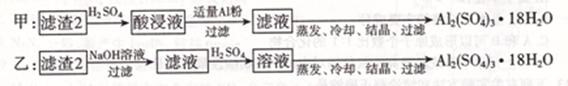
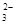 +I2= 2I-+S4O
+I2= 2I-+S4O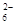
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com