
【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:

回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的净出率为70%时,所采用的实验条件为___________________。

(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O转化率% | 92 | 95 | 97 | 93 | 88 |
分析40℃时TiO2·xH2O转化率最高的原因__________________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02 mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L,此时是否有Mg3(PO4)2沉淀生成?___________(列式计算)。
FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式______。
【答案】 100℃、2h,90℃,5h FeTiO3+ 4H++4Cl = Fe2++ TiOCl42 + 2H2O 低于40℃,TiO2·xH2O转化反应速率随温度升高而增加;超过40℃,双氧水分解与氨气逸出导致TiO2·xH2O转化反应速率下降 4 Fe3+恰好沉淀完全时,c(PO43-)= ![]() mol·L1=1.3×10-17 mol·L1,c3(Mg2+)×c2(PO43-)=(0.01)3×(1.3×10-17)2=1.7×10-40<Ksp [Mg3(PO4)2],因此不会生成Mg3(PO4)2沉淀。 2FePO4 + Li2CO3+ H2C2O4
mol·L1=1.3×10-17 mol·L1,c3(Mg2+)×c2(PO43-)=(0.01)3×(1.3×10-17)2=1.7×10-40<Ksp [Mg3(PO4)2],因此不会生成Mg3(PO4)2沉淀。 2FePO4 + Li2CO3+ H2C2O4![]() 2LiFePO4+ H2O↑+ 3CO2↑
2LiFePO4+ H2O↑+ 3CO2↑
【解析】(1)由图示可知,“酸浸”时铁的净出率为70%时所需要的时间最短,速率最快,则应选择在100℃、2h,90℃,5h下进行;
(2)“酸浸”时用盐酸溶解FeTiO3生成TiOCl42时,发生反应的离子方程式为FeTiO3+4H++4Cl=Fe2++ TiOCl42 + 2H2O;
(3)温度是影响速率的主要因素,但H2O2在高温下易分解、氨水易挥发,即原因是低于40℃,TiO2·xH2O转化反应速率随温度升高而增加;超过40℃,双氧水分解与氨气逸出导致TiO2·xH2O转化反应速率下降;
(4)Li2Ti5O15中Li为+1价,O为-2价,Ti为+4价,过氧根(O22-)中氧元素显-1价,设过氧键的数目为x,根据正负化合价代数和为0,可知(+1)×2+(+4)×5+(-2)×(15-2x)+(-1)×2x=0,解得:x=4;
(5)Ksp[FePO4]=c(Fe3+)×c(PO43-)=1.3×10-2,则c(PO43-)= =1.3×10-17mol/L,Qc[Mg3(PO4)2]=c3(Mg2+)×c2(PO43-)=(0.01)3×(1.3×10-17)2=1.69×10-40<1.0×10—34,则无沉淀。
=1.3×10-17mol/L,Qc[Mg3(PO4)2]=c3(Mg2+)×c2(PO43-)=(0.01)3×(1.3×10-17)2=1.69×10-40<1.0×10—34,则无沉淀。
(6)高温下FePO4与Li2CO3和H2C2O4混合加热可得LiFePO4,根据电子守恒和原子守恒可得此反应的化学方程式为2FePO4 + Li2CO3+ H2C2O4![]() 2LiFePO4+ H2O↑+ 3CO2↑。
2LiFePO4+ H2O↑+ 3CO2↑。


科目:高中化学 来源: 题型:
【题目】填空:
(1)碱金属元素原子最外层的电子都是________个,在化学反应中它们容易失去________个电子。
(2)碱金属元素中还原性最强的是________,原子半径最小的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)有机物A、B、C、D、E之间发生如下的转化:
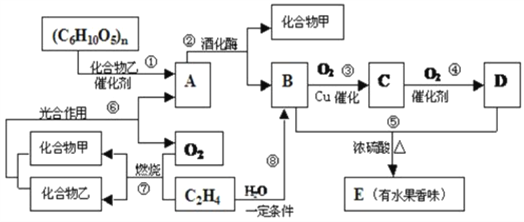
(1)写出C物质的结构简式:_________________;
(2)上述②~⑧转化反应中,属于取代反应的有____________;属于加成反应的有_______________________(用反应序号填写);
(3)向A的水溶液中加入新制的Cu(OH)2并加热时产生的实验现象是__________________________________________________________;
请写出下列转化的化学反应方程式:
(4)B + D → E:_______________________________________________;
(5)乙烯生成聚乙烯:__________________________________________;
(Ⅱ)己知葡萄糖在乳酸菌的作用下转化为乳酸,乳酸的结构简式为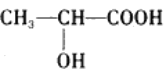 。
。
试回答:
(6)乳酸分子中含有________________和_______________两种官能团(写名称);
(7)乳酸与金属钠反应的化学方程式为_________________________________;
(8)足量乳酸与Na2CO3溶液反应的化学方程式为______________________________;
(9)乳酸在浓硫酸作用下,两分子相互发生酯化反应生成环状酯,此环状酯的结构简式为 ______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于钠的说法正确的是:
A. 4.6g钠溶于水所得溶液中.要使100个水分子溶有1个钠离子,需要水的质量是360g
B. 根据金属间置换的原理,把一小粒金属钠放入硫酸铜溶液中,可以生成金属铜
C. 当钠、钾等金属不慎着火时,可以用沙子扑灭、水浇灭等方法
D. 少量的金属钠长期暴露在空气中,它的最终产物是Na2CO3而不是NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有原子序数依次增大的A、B、C、D、E五种短周期元素和过渡元素F,其相关信息如表所示:
1 | A与C形成化合物的水溶液呈碱性 |
2 | B的最高正价与最低负价的代数和为0 |
3 | D的常见化合物的焰色反应为黄色 |
4 | E是同周期中简单离子半径最小的元素 |
(1)上述六种元素中,金属性最强的元素在周期表中的位置是__________________。
(2)分子式为B5Al2且其一氯代物只有一种的有机物的名称为_______________________。
(3)C元素的气态氢化物与其最高价氧化物对应的水化物化合生成M,M的水溶液呈______性;将M的浓溶液滴加到Mg(OH)2悬浊液中,描述现象并解释产生该现象的原因__________________。
(4)D元素的最高价氧化物对应的水化物与E元素的单质反应的离子方程式为_______________。
(5)F与B形成的合金在潮湿的空气中易发生电化学腐蚀形成红棕色固体,腐蚀过程中正极的电极反应式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由金属Na、Cu、C、N、B等元素组成的物质在生活和工业上有着广泛用途。
(1)基态Cu+的外围电子轨道式为_______。
(2)H3BNH3是储氢材料,其制备原理为:3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3,其中(HB=NH)3是一种六元环状化合物。化合物H3BNH3中B原子的杂化方式为_______;1个(HB=NH)3分子中含有 ___个σ键。
(3) B、C、N、O原子的第一电离能由大到小的顺序为_____________________。
(4)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为____(填字母)。
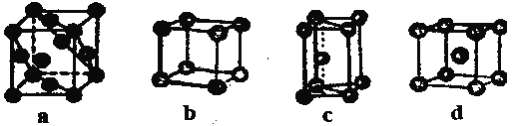
(5)已知NaCl的摩尔质量为Mg·mol-1,密度为pg·㎝-3,阿伏加德罗常数为NA mol-1,在NaCl晶体中,两个距离最近的Cl-中心间的距离为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】凯氏定氨法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量。已知:
NH3+H3BO3=NH3·H3BO3;
NH3·H3BO3+HCl= NH4Cl+ H3BO3。

回答下列问题:
(1)a的作用是_______________。
(2)b中放入少量碎瓷片的目的是____________。f的名称是__________________。
(3)清洗仪器:g中加蒸馏水:打开k1,关闭k2、k3,加热b,蒸气充满管路:停止加热,关闭k1,g中蒸馏水倒吸进入c,原因是____________;打开k2放掉水,重复操作2~3次。
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂,铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭k3,d中保留少量水,打开k1,加热b,使水蒸气进入e。
①d中保留少量水的目的是___________________。
②e中主要反应的离子方程式为________________,e采用中空双层玻璃瓶的作用是________。
(5)取某甘氨酸(C2H5NO2)样品m 克进行测定,滴定g中吸收液时消耗浓度为cmol·L-1的盐酸V mL,则样品中氮的质量分数为_________%,样品的纯度≤_______%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是进行化学研究的重要环节,下列有关化学实验的说法错误的是
A. 用酒精灯外焰加热铝箔,铝箔熔化但不滴落,说明Al2O3的熔点比Al的熔点高
B. 可用勒夏特列原理解释2NO2(g)![]() N2O4(g)体系加压后颜色变深
N2O4(g)体系加压后颜色变深
C. 用酸性KMnO4溶液验证草酸的还原性
D. 向滴有KSCN的FeCl3溶液中加入NaOH溶液以研究反应物浓度对化学平衡的影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com