
【题目】下列叙述中正确的是
A. 直径介于l~100 nm之间的粒子被称为胶体
B. 电泳现象可证明胶体带电荷
C. 利用丁达尔现象可区别溶液和胶体
D. 胶体粒子很小,但不能通过滤纸
科目:高中化学 来源: 题型:
【题目】有Al、CuO、Fe2O3组成的混合物共10.0g,放入250mL某浓度的硫酸溶液中,混合物完全溶解,当再加入125mL 2.00mol/L的NaOH溶液时,得到沉淀物质的量最多.上述硫酸溶液的浓度为( )
A.0.500 mol/L
B.1.00 mol/L
C.2.00 mol/L
D.3.00 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
A | 578 | 1817 | 2745 | 11578 |
B | 738 | 1451 | 7733 | 10540 |
A通常显价,B元素的核外电子排布式为。
(2)波长为300nm紫外光的光子所具有的能量约为399 kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因是。组成蛋白质的最简单的氨基酸中的碳原子杂化类型是。
共价键 | C-C | C-N | C-S |
键能/ kJ·mol-1 | 347 | 305 | 259 |
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构
与NaCl晶体结构相似(如下图所示),已知3种离子晶体的晶格能数据如下表: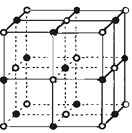
离子晶体 | NaCl | KCl | CaO |
晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是。其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有个。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是。
(5)某配合物的分子结构如下图所示,其分子内不含有(填序号)。
A.离子键
B.极性键
C.金属键
D.配位键
E.氢键
F.非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关水的电离的说法正确的是
A.将水加热,KW增大,pH不变
B.向水中加入少量NaHSO4固体,恢复到原温度,水的电离程度增大
C.向水中加入少量NH4Cl固体,恢复到原温度,水的电离程度减小
D.向水中加少量NaOH固体,恢复到原温度,水的电离被抑制,[OH-]增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.二氧化锰和浓盐酸反应:MnO2+4HCl(浓) ![]() ?Mn2++2Cl2↑+2H2O
?Mn2++2Cl2↑+2H2O
B.稀盐酸和硅酸钠溶液反应:SiO32﹣+2H+═H2SiO3↓
C.碳酸钙和稀盐酸反应:CO32﹣+2H+═CO2↑+H2O
D.铜和氯化铁溶液反应:Fe3++Cu═Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N﹣N﹣N键角都是108.1°,下列有关N(NO2)3的说法正确的是( ) 
A.分子中N,O间形成的共价键是非极性键
B.分子中四个氧原子共平面
C.该物质既有氧化性又有还原性
D.15.2g该物质含有6.02×1022个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“玉兔”号月球车用 ![]() Pu作为热源材料,下列关于
Pu作为热源材料,下列关于 ![]() Pu的说法正确的是( )
Pu的说法正确的是( )
A.![]() Pu与
Pu与 ![]() U互为同位素
U互为同位素
B.![]() Pu与
Pu与 ![]() Pu具有相同的中子
Pu具有相同的中子
C.![]() Pu与
Pu与 ![]() U具有完全相同的化学性质
U具有完全相同的化学性质
D.![]() Pu与
Pu与 ![]() Pu具有相同的最外层电子
Pu具有相同的最外层电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com