
设NA为阿伏德罗常数的值,下列叙述正确的是
A.常温常压下,23g的NO2含有的氧原子数目为NA
B.已知某种元素的一种原子的质量为ag,则该元素的相对原子质量近似为aNA
C.某密闭容器盛有0.1molN2和0.4molH2,在一定条件下充分反应,转移电子的数目为0.6NA
D.80gNH4NO3晶体中含有NH4+小于NA
科目:高中化学 来源:2015-2016学年四川省高二上10月月考化学试卷(解析版) 题型:填空题
(18分)A、B、C、D、E、F为原子序数依次增大的短周期元素,G为第四周期元素,B、C相邻且同周期,A、D同主族。A、C能形成两种化合物甲和乙,原子个数比分别为2∶1和1∶1,甲为常见的溶剂。E是地壳中含量最多的金属元素。F元素为同周期电负性最大的元素。D和F可形成化合物丙,E和F可形成化合物丁。G为第四周期未成对电子数最多的元素。请回答下列问题:
(1)写出G基态原子的电子排布式
(2)B和C比较,第一电离能较大的元素是 (填元素符号),其原因为
(3)A与B形成的化合物易溶于化合物甲,其主要原因是
(4)甲、乙两分子中含有非极性共价键的是 (填分子式),它中心原子的杂化方式是
(5)已知化合物丁熔点190℃,沸点183℃,结构如右图所示。
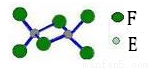
①丙和丁比较,熔点较低的化合物是 (填化学式),其原因为
②则丁含有的作用力有 (填序号)。
A.离子键 B.共价键 C.金属键
D.配位键 E.范德华力
查看答案和解析>>
科目:高中化学 来源:2016届山东省南校区高三上学期10月阶段测化学试卷(解析版) 题型:选择题
将铁铝矾[Al2Fe(SO4)4·xH2O]溶于水中,得到浅绿色溶液,有关该溶液的叙述正确的是
A.铁铝矾有净水作用,其水溶液显中性
B.向该溶液中加入Na2S溶液,有淡黄色沉淀
C.在空气中,蒸干并灼烧该溶液,最后所得的残留固体为Al2O3、Fe2O3
D.用惰性电极电解该溶液时,阴极区有沉淀
查看答案和解析>>
科目:高中化学 来源:2016届湖南省常德市高三上学期第三次月考化学试卷(解析版) 题型:推断题
(10分)已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现红色。
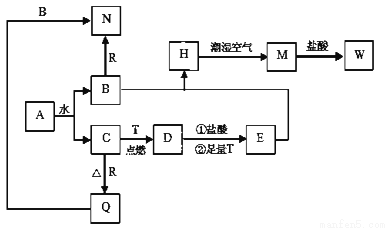
(1)写出下列物质的化学式:A:______________ D________________
(2)按要求写出下列反应的化学方程式:
H在潮湿空气中变成M的实验现象为___________________,
该过程用化学方程式可表示为:________________________。
(3)B和R反应生成N的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期10月月考化学试卷(解析版) 题型:填空题
(Ⅰ)四种短周期元素A、B、C、D的性质或结构信息如下:
①原子半径:A>B>C>D
②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲: 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二
乙: 无色,无气味并且易燃.是常见的一种基础能源
无色,无气味并且易燃.是常见的一种基础能源
丙: 有强氧化性的弱酸,可以用于消毒杀菌
有强氧化性的弱酸,可以用于消毒杀菌
请根据上述信息回答下列问题.
(1)B元素在周期表中的位置第二周期_______________,请写出BC2分子的结构式_____________。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂.E单质与甲反应有化合物X生成.请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生的离子反应方程式_____________________。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生的离子反应方程式为_________________________。
(Ⅱ)某研究小组将CaCl2和H2在一定条件下反应,制得两种化合物(甲和乙).元素组成分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%;化合物乙的水溶液显酸性.请回答下列问题:
(1)甲的电子式是_________________。
(2)甲与乙溶液反应可得H2,其化学方程式是_____________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古巴彦淖尔高二上10月月考化学试卷(解析版) 题型:选择题
在测定中和热的实验中,下列说法正确的是
A.使用环形玻璃棒是为了加快反应速率,减小实验误差
B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触
C.用0.5mol·L-1NaOH溶液分别与0.5 mol·L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同
D.在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古巴彦淖尔高一上10月月考化学试卷(解析版) 题型:选择题
下列有关气体摩尔体积的描述中正确的是
A.单位物质的量的气体所占的体积叫做气体摩尔体积
B.通常状况下的气体摩尔体积约为22.4L
C.标准状况下的气体摩尔体积约为22.4L
D.相同物质的量的气体摩尔体积也相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上学期9月月考化学试卷(解析版) 题型:选择题
Na2S2O3溶液跟稀H2SO4反应的化学方程式为:
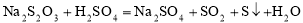 。下列各组实验中,溶液中最先变浑浊的是
。下列各组实验中,溶液中最先变浑浊的是
反应 | 反 应 物 | H2O | ||||
温度 | Na2S2O3 | H2SO4 | V | |||
℃ | v(mL) | c(mol?L-1) | v(mL) | c(mol?L-1) | (mL) | |
A | 10 | 5 | 0.1 | 10 | 0.1 | 5] |
B | 10 | 5 | 0.1 | 5 | 0.1 | 10 |
C | 30 | 5 | 0.1 | 5 | 0.1 | 10 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上期中考试化学试卷(解析版) 题型:选择题
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。RFC的工作原理如图所示。下列有关说法正确的是
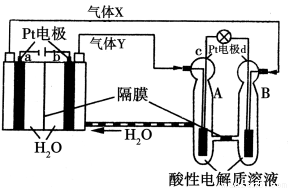
A.当有0.1 mol电子转移时,a电极产生2.24 L H2
B.b电极上发生的电极反应式为4H2O+4e-===2H2↑+4OH-
C.c电极上进行还原反应,B池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应式为O2+4H++4e-===2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com