
为验证氧化性Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和 A中加热装置已略,气密性已检验)。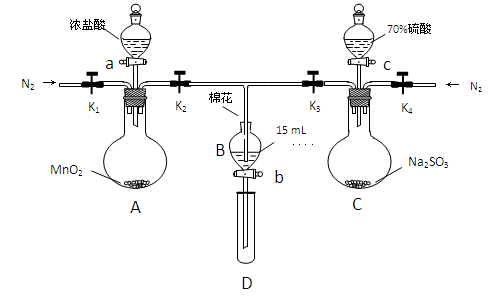
实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)A中发生反应的化学方程式为 。
(2)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是 。
(3)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性
Cl2>Fe3+>SO2的是 (填“甲”“乙”“丙”)。
| | 过程Ⅳ B溶液中含有的离子 | 过程Ⅵ B溶液中含有的离子 |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
 FeSO3(s)(墨绿色)
FeSO3(s)(墨绿色)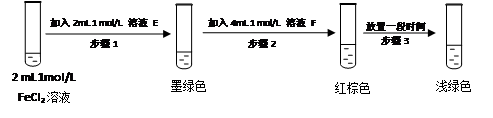
(1)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O (2分)
MnCl2+Cl2↑+2H2O (2分)
(2)70%的硫酸中c(H+)比98%的硫酸大,因此反应速率更快。(2分)
(3)乙、丙 (2分)
(4)① Na2SO3(或可溶性亚硫酸盐)、FeCl3 (2分,各1分)
② Fe3+ 消耗 SO32-,c(SO32-)减小,使平衡Fe2+(aq)+SO32-(aq) FeSO3(s)逆向移动,溶液颜色由红棕色变为浅绿色 (2分)
FeSO3(s)逆向移动,溶液颜色由红棕色变为浅绿色 (2分)
解析试题分析:
⑵反应速率的影响因素有温度、浓度、催化剂、接触面积等,该题中只有浓度不同,浓硫酸溶液中溶质主要以硫酸分子形式存在,电离出的氢离子少、浓度低。
⑶该题的理论依据是氧化还原反应中氧化剂的氧化性强于氧化产物,也强于还原剂的氧化性;甲、B可能有存在溶解的氯气氧化二氧化硫;乙、B中存在二价铁离子三价铁离子,说明氯气的氧化性强于三价铁离子,且没有氯气剩余;故后有硫酸根离子能说明三价铁离子氧化性强于二氧化硫;丙、B中存在三价铁离子,说明氯气氧化性强于三价铁离子;后生成了二价铁离子,只能是三价铁离子被二氧化硫还原,正确。
⑷根椐假设和实验应先生成亚硫酸铁,再和三氯化铁混合,所以分别加入亚硫酸钠溶液、氯化铁溶液;溶液变为浅绿色说明生成了二价铁离子,即2Fe3++SO32-+H2O=2Fe2++SO42-+2H+促使2Fe3++3H2O Fe(OH)3+3H+和SO32-+H2O
Fe(OH)3+3H+和SO32-+H2O HSO32-+OH-逆向进行,溶液变为浅绿色。
HSO32-+OH-逆向进行,溶液变为浅绿色。
考点:综合化学实验题,考查实验的具体操作步骤、操作目的、原理、微粒的检验以及分析等有关问题。


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:填空题
实验室模拟用工业废弃固体(含有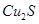 、Al2O3、Fe2O3、SiO2等)制取粗铜、绿矾(
、Al2O3、Fe2O3、SiO2等)制取粗铜、绿矾(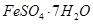 )和明矾[Kal(SO4)2
)和明矾[Kal(SO4)2 12H2O]的操作流程如下:
12H2O]的操作流程如下: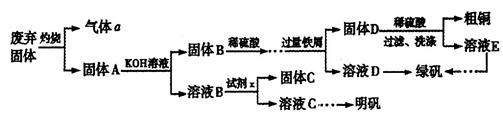
(1)试剂x是_________(写化学式)。
(2)配平下列方程式:
____
(4)为了分析产品(绿矾)中铁元素的含量,某同学称取20.0g样品配成100mL溶液,移取25.00mL用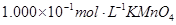 标准溶液进行滴定(MnO
标准溶液进行滴定(MnO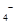 被还原为
被还原为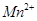 )。
)。
请回答下列问题:
①滴定时,KmnO4标准溶液应盛放在______________(填仪器名称)中。
②若达到滴定终点消耗KmnO4标准溶液体积为25.00mL,则该产品中铁元素的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(18分)为验证氧化性Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和 A中加热装置已略,气密性已检验)实验过程如下:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是_________________________________________________。
(2)棉花中浸润的溶液为______________________。
(3)A中发生反应的化学方程式为 。
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是 。
(5)能说明氧化性Fe3+>SO2的离子方程式是______________________________________。
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是 (填“甲”“乙”“丙”)。
| | 过程Ⅳ B溶液中含有的离子 | 过程Ⅵ B溶液中含有的离子 |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
 FeSO3(s)(墨绿色)
FeSO3(s)(墨绿色)
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某同学为了验证Fe3+是否能氧化H2SO3生成SO,他用50 mL 0.1 mol·L-1 FeCl3溶液吸收制取SO2气体的尾气后,进行以下实验:
(1)检验吸收液中的SO42—:_____________________________,
证明Fe3+能够把H2SO3氧化成SO42—。
(2)请完成并配平上述反应中的化学方程式:
2FeCl3+SO2+________===________+H2SO4+________,反应中的氧化产物是________(写化学式)。
(3)吸收液中除了含有H+、Cl-、SO42—以外,对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①提出假设。假设1:溶液中存在Fe3+、Fe2+;
假设2:溶液中存在________。
②设计方案,进行实验,验证假设。请写出实验步骤以及预期现象和结论(可不填满)。
限选实验试剂和仪器:试管、滴管、0.1 mol·L-1KMnO4溶液、0.1 mol·L-1KSCN溶液、品红稀溶液。
| 实验步骤 | 预期现象和结论 |
| 步骤1:用试管取样品溶液2~3 mL,再用滴管取_________ | 若出现红色,则假设1成立;若未出现红色,则假设1不成立(或假设2成立) |
| 步骤2: | |
| 步骤3: | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验: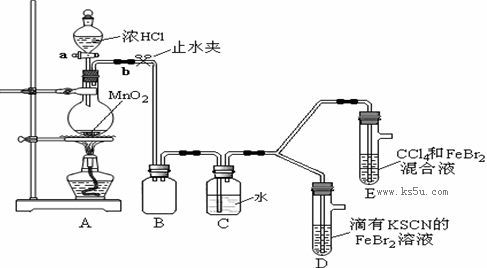
①检查气体发生装置A的气密性的操作是 。
②整套实验装置存在一处明显的不足,请指出: 。
(2)用改正后的装置进行实验,实验过程如下:
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯。 | D装置中:溶液变红 E装置中:水层溶液变黄, 振荡后,CCl4层无明显变化。 | Cl2、Br2、Fe3+的氧化性由强到弱的顺序为: |
| ⅰ.(SCN)2性质与卤素单质类似。氧化性:Cl2>(SCN)2。 ⅱ.Cl2和Br2反应生成BrCl,它呈红色(略带黄色),沸点约5℃,与水发生水解反应。 ⅲ.AgClO、AgBrO均可溶于水。 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
实验记录如下:
| | 实验操作 | 实验现象 |
| I | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为红棕色。 |
| II | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化。 |
| III | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色。 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某校研究小组为探究KI溶液的pH与其在空气之中氧化变质的关系,进行了相应的实验探究。
【提出假设】
假设1:只有碱性环境下能被氧化
假设2:只有酸性环境下能被氧化
假设3:只有中性环境下能被氧化
假设4: 能被氧化
【实验探究】
(1)有人认为由于I2会和KOH反应,因此否定假设1。小组同学认为,若溶液的碱性较弱时,I2不会反应。为了验证滚点,小组同学进行了下述实验:
在编号为①②③的试管中加入相同量的碘的淀粉溶液中,然后分别加入pH为9、10、11的KOH溶液,发现试管①中蓝色不消失,试管②③中蓝色消失。
由此可以得出结论: 。
(2)为探究KI溶液在不同碱性条件下能否被氧气氧化,小组同学设计了以下实验:将下表中的药品分别加入到试管中,然后放置于收集有氧气的储气瓶中,塞上塞子,观察现象。完成以下实验设计表(表中不要留空格)。
| 实验编号 | 蒸馏水 | 淀粉溶液 | KI固体 | 稀KOH溶液 | 一段时间后观察实验现象 |
| 1 | 30mL | 2 mL | 5g | 0滴 | 试管中出现了蓝色 |
| 2 | 29.5 mL | | 5g | 10滴 | 试管中出现了很浅的淡蓝色 |
| 3 | 29 mL | 2 mL | | 20滴 | 试管中无明显变化 |
| 4 | | 2 mL | 5g | 30滴 | |
| 实验方案(不要求写具体过程) | 预期实验结果和结论 |
| | |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于Na、Mg及其化合物的说法正确的是
| A.钠在空气中燃烧生成Na2O |
| B.点燃的镁条在CO2中燃烧,生成氧化镁和碳 |
| C.钠保存在酒精中是因为酒精不与钠发生反应,且酒精的密度比钠小 |
| D.足量稀HCl加入Mg(OH)2沉淀中,加热蒸干得无水MgCl2固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com