
ʵ����ģ���ù�ҵ�������壨����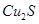 ��Al2O3��Fe2O3��SiO2�ȣ���ȡ��ͭ���̷���
��Al2O3��Fe2O3��SiO2�ȣ���ȡ��ͭ���̷���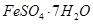 ����������Kal��SO4��2
����������Kal��SO4��2 12H2O�ݵIJ����������£�
12H2O�ݵIJ����������£�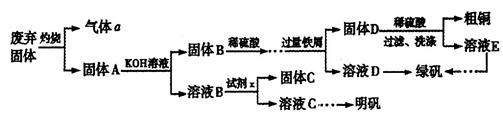
��1���Լ�x��_________��д��ѧʽ����
��2����ƽ���з���ʽ��
____
��4��Ϊ�˷�����Ʒ���̷�������Ԫ�صĺ�����ijͬѧ��ȡ20.0g��Ʒ���100mL��Һ����ȡ25.00mL��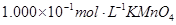 ����Һ���еζ���MnO
����Һ���еζ���MnO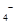 ����ԭΪ
����ԭΪ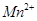 ����
����
��ش��������⣺
�ٵζ�ʱ��KmnO4����ҺӦʢ����______________�����������ƣ��С�
�����ﵽ�ζ��յ�����KmnO4����Һ���Ϊ25.00mL����ò�Ʒ����Ԫ�ص���������Ϊ_________��
��1��H2SO4����KHSO4����2�֣�
��2������Ũ���������Ũ������Ũ��������ȴ�ᾧ��4�֣�
��3��2��5��2��2��5��4��3�֣�
��4������ʽ�ζ��ܣ�2�֣� ��14%��3�֣�
���������������1������KOH����ҺB����K[Al(OH)4],��������Ϊ����������XΪH2SO4����KHSO4����
��3�����ݻ��ϼ�������������ƽ��ѧ����ʽ��
��4���ٸ�����ؾ���ǿ�����ԣ��������ܣ�ֻ��ʢ������ʽ�ζ����У�
�ڸ��ݵ����غ��֪��KMnO4��5Fe2+,20.0��Ʒ�к�����0.025L��0.1mol/L��5��4��56g/mol=2.8g�����������Ԫ�ص�����������
���㣺���⿼��������ͼ���������ӷ���ʽ����ƽ���ζ�����ѧ���㡣


 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�������ȣ�ClO2��Ϊһ�ֻ���ɫ���壬�ǹ����Ϲ��ϵĸ�Ч�����ס����١���ȫ��ɱ����������
��1����ҵ���Ʊ�ClO2�ķ�Ӧԭ�������ã�2NaClO3��4HCl=2ClO2����Cl2����2H2O��2NaCl��
��Ũ�����ڷ�Ӧ����ʾ������������_______������ţ���
| A��ֻ�л�ԭ�� | B����ԭ�Ժ����� | C��ֻ�������� | D�������Ժ����� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��Ԫ������Ȼ������Ҫ��������������Ҫ�ɷ�ΪAl2O3��������Fe2O3��FeO��SiO2���С���ҵ�����������Ʊ�����ij�ֻ�����Ĺ����������¡�
��1������ҺA�м���Ư��Һ��Ŀ��������������������ҺB�����ԡ�
�ٸù������漰ij������ԭ��Ӧ���£�����ɣ�
��Fe2++��ClO��+�� =��Fe(OH)3��+��C1��+��
�ڼ�����ҺB���Ƿ�����Ԫ�صķ���Ϊ��
��ע���Լ�������
�۽���ҺB�е���Ԫ���Գ�����ʽ��������ѡ�õ�����Լ�Ϊ ������ţ���
a������������Һ b��������Һ c����ˮ d��������̼
������ҺB�Ʊ��Ȼ��������漰�IJ���Ϊ���ߵμ�Ũ���������Ũ������ȴ�ᾧ�� ����������ƣ���ϴ�ӡ�
��2��SiO2��NaOH�����Ʊ������ƣ��ɲ��õ�װ��Ϊ ������ţ���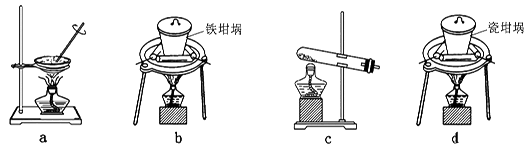
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��������̼�ܵ����Ƴɹ������˿Ƽ��Ľ������õ绡���ϳɵ�����̼�ܳ����д���������̼������������̼���������������������ᴿ���䷴Ӧ�еķ�Ӧ�����������C��CO2��H2SO4��K2Cr2O7��K2SO4��Cr2(SO4)3��H2O�������ʡ�
��1����������������գ�����ƽ��ѧ����ʽ��
��2��������Ӧ����������(�ѧʽ)_______________����������Ԫ����(��Ԫ�ط���)_____________��
��3��H2SO4��������Ӧ�б��ֳ�����������(��ѡ����)____________________��
A�������� B������ C�������Ժ����� D����ԭ�Ժ�����
��4������Ӧ�е���ת����0.8 mol��������������ڱ�״���µ����Ϊ________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���������һ�ֵ��͵�ǿ��������
���������գ�
������KMnO4������Һ����Cu2S��CuS�Ļ����ʱ�������ķ�Ӧ���£�
�� MnO4��+ Cu2S + H+�� Cu2+ + SO2�� + Mn2+ + H2O(δ��ƽ)
�� MnO4��+ CuS + H+ �� Cu2+ + SO2�� + Mn2+�� H2O(δ��ƽ)
��1�����й��ڷ�Ӧ�ٵ�˵���д������ ��ѡ���ţ���
a����������Ԫ����Cu��S
b���������뻹ԭ�������ʵ���֮��Ϊ8:5
c������2.24 L(�����) SO2��ת�Ƶ��ӵ����ʵ�����0.8 mol
d����ԭ�Ե�ǿ����ϵ�ǣ� Mn2+> Cu2S
��2�������Ӧ���е���ת�Ƶķ������Ŀ�� MnO4��+ CuS
����ϡ�����У�MnO4����H2O2Ҳ�ܷ���������ԭ��Ӧ
������Ӧ��H2O2��2e �� 2H+ + O2��
��ԭ��Ӧ��MnO4�� + 5e + 8H+ �� Mn2+ + 4H2O
��3����Ӧ������0.5 mol H2O2�μӴ˷�Ӧ��ת�Ƶ��ӵĸ���Ϊ ����������Ӧ�ó�������������ǿ���Ľ����� >___________(��д��ѧʽ)��
��4����֪��2KMnO4+ 7H2O2+3H2SO4�� K2SO4+2MnSO4 +6O2��+10H2O����1mol KMnO4������H2O2��
mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ƺ�ݳ��ѳ�Ϊһ��������⡣����ʻ��Ա�����оƾ�Ũ�ȣ�BrAC���ķ����ж��֡�
��1�����������ü���Լ���ɫ�仯�����ж�BrAC���������·�Ӧ���BrAC��
3CH3CH2OH��2KMnO4��3CH3CHO��2MnO2��2KOH��2H2O ��
������Ӧ�з�����ԭ��Ӧ�Ĺ�����________ ��_________��
��2����������������������������������ĵ�����Һ���BrAC����Һ�������Ҵ�������Ϊ��ȩ���÷�Ӧ�Ļ�ѧ����ʽΪ_________��
��3��1994�������״���ʹ����Һ�ƾ�������ⷽ������ΪѪҺ������֮��ĵ����ּ���ֶΡ���ԭ�������Ҵ�����ø�����£��Ҵ���������Ӧ������ȩ�������⣬�жϸ��������Ҵ�����������ȩ��������������������������ǿ��������_______����д��ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ����Լ�ȼ�ϵĿ�������������Ҫ���塣
��1��NO2����ˮ���գ����÷�Ӧ6NO2+8NH3 7N2+12H2O��
7N2+12H2O��
Ҳ���Դ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������______________L��
��2����֪��2SO2(g)+ O2 (g)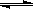 2SO3 (g)������H =��196.6kJ��mol��1
2SO3 (g)������H =��196.6kJ��mol��1
2NO(g)+ O2 (g) 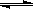 2NO2 (g)������H =��113.0kJ��mol��1
2NO2 (g)������H =��113.0kJ��mol��1
��ӦNO2(g)+ SO2 (g) 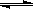 SO3 (g) +NO(g)�ġ�H =______kJ��mol��1
SO3 (g) +NO(g)�ġ�H =______kJ��mol��1
��3��CO�����ںϳɼ״�����Ӧ����ʽΪCO(g)+ 2H2 (g) 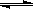 CH3OH (g)���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ����������������غ�﮵�ص�10����������ʹ��1���³��һ�Ρ��ٶ��ŵ�����У��״���ȫ����������CO2�������������CO32��
CH3OH (g)���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ����������������غ�﮵�ص�10����������ʹ��1���³��һ�Ρ��ٶ��ŵ�����У��״���ȫ����������CO2�������������CO32��
�ٸõ�ط�Ӧ�������ӷ���ʽΪ____________________________________________��
�ڼ״���____��������Ӧ��������������ڷŵ��������Һ��pH��____________����ͻ����������䣩������16�˼״���������ȫ����,�����ĵ��ܵ��������CuSO4��Һ����������������������������Ϊ80������������״���µ�O2________________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��6�֣���50mL a mol��L-1��������Һ�У�����6.4g Cu��ȫ���ܽ⣬��������Ļ�ԭ����ֻ��NO2��NO������Ӧ����Һ������ˮϡ����100mLʱ���c(NO3-)="3" mol��L-1��
��1����ϡ�ͺ����Һ��pH= ��
��2����a=9�������ɵ�������NO2�����ʵ���Ϊ mol��
��3����������������Ⱦ�ķ���֮һ����NaOH��Һ�������գ���Ӧԭ�����£�
NO2+NO+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
����������NO2��NO�Ļ������ͨ��1mol��L-1��NaOHǡ�ñ����գ���NaOH��Һ�����Ϊ mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
Ϊ��֤������Cl2��Fe3+��SO2��ijС������ͼ��ʾװ�ý���ʵ�飨�г������� A�м���װ�����ԣ��������Ѽ��飩��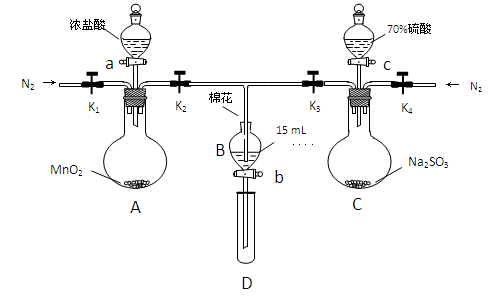
ʵ����̣�
��.���ɼ�K1~K4��ͨ��һ��ʱ��N2���ٽ�T�͵��ܲ���B�У�����ͨ��N2��Ȼ��ر�K1��K3��K4��
��.����a���μ�һ������Ũ���ᣬ��A���ȡ�
��.��B����Һ���ʱ��ֹͣ���ȣ��н����ɼ�K2��
��.����b��ʹԼ2mL����Һ����D�Թ��У��������е����ӡ�
��.���ɼ�K3������c������70%�����ᣬһ��ʱ���н����ɼ�K3��
��.�����Թ�D���ظ����̢�������B��Һ�е����ӡ�
��1��A�з�����Ӧ�Ļ�ѧ����ʽΪ ��
��2����70%��������ȡSO2����Ӧ���ʱ���98%������죬ԭ���� ��
��3���ס��ҡ�����λͬѧ�ֱ����������ʵ�飬���ǵļ����һ���ܹ�֤��������
Cl2��Fe3+��SO2���� ����ס����ҡ�����������
| | ���̢� B��Һ�к��е����� | ���̢� B��Һ�к��е����� |
| �� | ��Fe3+��Fe2+ | ��SO42- |
| �� | ����Fe3+����Fe2+ | ��SO42- |
| �� | ��Fe3+��Fe2+ | ��Fe2+ |
 FeSO3��s����ī��ɫ��
FeSO3��s����ī��ɫ��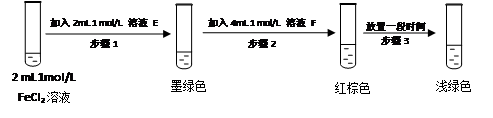
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com