
【题目】下列说法正确的是( )
A. 甲烷的标准燃烧热为ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. CO(g)的燃烧热是283.0 kJ·mol-1,则CO2分解的热化学方程式为:2CO2(g)===2CO(g)+O2(g) ΔH=+283.0 kJ·mol-1
C. 一定条件下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
D. 同温同压下,反应H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH相同
科目:高中化学 来源: 题型:
【题目】铝镁合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要有于制作窗框、卷帘门、防护栏等.下列与这些用途无关的性质是( )
A.导电性好
B.不易生锈
C.光泽度好
D.强度高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+I2(g)![]() 2HI(g)△H<0。相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。下列说法错误的是
2HI(g)△H<0。相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。下列说法错误的是
A. 反应放出的热量一定相同 B. 此时体系的压强一定相同
C. 反应物的转化率可能相同 D. 此时HI的浓度一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式____________________。

(2)已知:
N2(g)+O2(g)=2 NO(g) △H=+180 kJ·mol-1
2NO(g)+2 CO(g)=N2(g)+2 CO2(g)△H=-746 kJ·mol-1
则反应CO(g)+1/2O2(g)=CO2(g)的△H=________kJ·mol-1。
(3)在一固定容积为2L的密闭容器内加人0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应。N2(g)+3H2(g)![]() 2NH3(g)△H<0,若第5min时达到平衡,此时测得NH3的物质的量为0.2mol,则前5min的平均反应速率v(N2)为_________,平衡时H2的转化率为_________,该反应的平衡常数K=__________(计算结果保留一位小数)。
2NH3(g)△H<0,若第5min时达到平衡,此时测得NH3的物质的量为0.2mol,则前5min的平均反应速率v(N2)为_________,平衡时H2的转化率为_________,该反应的平衡常数K=__________(计算结果保留一位小数)。
(4)在固定体积的密闭容器中,1.0×103kPa时,反应N2(g)+3H2(g)![]() 2NH3(g) △H <0的平衡常数K与温度T的关系如下表:则K1_________K2(填写“>”、“=”或“<”)
2NH3(g) △H <0的平衡常数K与温度T的关系如下表:则K1_________K2(填写“>”、“=”或“<”)
T/K | 298 | 398 | 498 |
平衡常数K | 51 | K1 | K2 |
(5)在体积一定的密闭容器中能说明合成氨反应一定达到平衡状态的是____(填字母)
a.容器内N2、H2、NH3的浓度之比为1︰3︰2
b.NH3的浓度保持不变
c.容器内压强保持不变
d.混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从南方往北方长途运输水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液的氧化性,催熟水果
D.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷与KOH水溶液反应,主要产物是________________,化学反应方程式是____________________;该反应属于____________反应。
溴乙烷与KOH乙醇溶液共热,主要产物是________________,化学反应方程式是____________________;该反应属于____________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家发明的水溶液锂电池为电动汽车发展扫除了障碍,装置原理如下图所示,其中固体薄膜只允许Li+通过。锂离子电池的总反应为xLi +Li1-xMn2O4![]() LiMn2O4,下列有关说法错误的是
LiMn2O4,下列有关说法错误的是
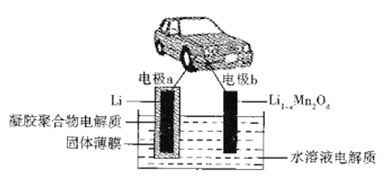
A. 放电时,Li+穿过固体薄膜进入到水溶液电解质中
B. 放电时,正极反应为Li1-xMn2O4+xLi++xe-![]() LiMn2O4
LiMn2O4
C. 该电池的缺点是存在副反应:2Li +2H2O![]() 2LiOH+H2↑
2LiOH+H2↑
D. 充电时,电极b为阳极,发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列方程式
(1)制溴苯__________________________________________________
(2)制TNT__________________________________________________
(3)由乙炔制聚氯乙烯_______________________________________________________________________________________________________
(4)60℃时1,3—丁二烯与溴水的1,4—加成反应
___________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com