
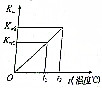
 ˮ�����ӻ�����Kw���¶�t���棩�Ĺ�ϵ��ͼ��ʾ��
ˮ�����ӻ�����Kw���¶�t���棩�Ĺ�ϵ��ͼ��ʾ��| 10-12 |
| 0.1 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��Na+����c��CH3COOH����c��CH3COO-�� |
| B��c��Na+����c��CH3COO-����c��OH-����c��H+�� |
| C��c��Na+��=c��CH3COOH��+c��CH3COO-�� |
| D��c��Na+��+c��H+��=c��CH3COO-��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c1��c2=1��3 |
| B��c1��ȡֵ��ΧΪ0��c1��0.14 |
| C��X��Y��ת������� |
| D��ƽ��ʱ��Y��Z����������֮��2��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��X���������������� |
| B��X������һ�����в����ͼ� |
| C��X������һ������n��̼ԭ�ӣ�2n����ԭ�ӣ�������ȷ��Oԭ����Ŀ |
| D��X��������������ԭ�ӣ�������X������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 A��ij�����Ͼɻ�е�����Ϻ�ɫ�������Ҫ�ɷ�Fe2O3��B��C��F���ǵ��ʣ�D��F������ɫ��ζ�����壬����֮����ת����ϵ��ͼ��ʾ����ش�
A��ij�����Ͼɻ�е�����Ϻ�ɫ�������Ҫ�ɷ�Fe2O3��B��C��F���ǵ��ʣ�D��F������ɫ��ζ�����壬����֮����ת����ϵ��ͼ��ʾ����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 25��ʱ����20mLϡ��������μ���0.1mol?L-1�İ�ˮ�������Һ��pH����백ˮ������仯��ͼ��ʾ������������ȷ���ǣ�������
25��ʱ����20mLϡ��������μ���0.1mol?L-1�İ�ˮ�������Һ��pH����백ˮ������仯��ͼ��ʾ������������ȷ���ǣ�������| A��x=20 |
| B��ϡ�����Ũ��Ϊ0.1mol?L-1 |
| C��a��ʱ�У�c��NH4+����2c��SO42-�� |
| D��b���ʾϡ����Ͱ�ˮǡ���к� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Cu��OH��2 |
| B��Cu��OH��2?CuSO4 |
| C��2Cu��OH��2?CuSO4 |
| D��3Cu��OH��2?CuSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��MnO4-��H+����������Fe2+�ǻ�ԭ�� |
| B��H2O�������������ǻ�ԭ�� |
| C��ÿ����1molˮת��1.2mol�ĵ��� |
| D��Fe2+�Ļ�ԭ��ǿ��Mn2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����NaHCO3��Һ�У�K+��Cl-��CH3COO-��C6H5O- |
| B����pH=13����ɫ��Һ�У�K+��Na+��I-��Cr2O72- |
| C�����Ȼ�ɫ����Һ�У�Na+��Al3+��NO3-��F- |
| D��1.0mol?L-1��KCl����Һ�У�H+��Ag+��SO42-��NO3- |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com