
| A、X可能属于糖类物质 |
| B、X分子中一定含有不饱和键 |
| C、X分子中一定含有n个碳原子,2n个氢原子,但不能确定O原子数目 |
| D、X分子中若含有氧原子,则常温下X不可能是气体 |


 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
 某兴趣小组设计如下微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是( )
某兴趣小组设计如下微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是( )A、断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl-
| ||||
| B、断开K2,闭合K1时,铜电极附近溶液变红 | ||||
| C、断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e-=2Cl- | ||||
| D、断开K1,闭合K2时,石墨电极作负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸和硬脂酸互为同系物,C2H6和C9H20也一定互为同系物 |
| B、化学式分别为C6H12O和C8H10O的两种芳香族化合物一定互为同系物 |
| C、甘氨酸和丙氨酸缩合最多可形成3种二肽 |
| D、2,2,3,3-四甲基丁烷可以由烯烃加氢转化而来 |
查看答案和解析>>
科目:高中化学 来源: 题型:
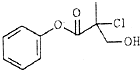
| A、有机物A属于芳香烃 |
| B、有机物A分子式为:C10H8O3Cl |
| C、有机物A和浓硫酸混合加热,可以发生消去反应 |
| D、1molA和足量的NaOH溶液反应,最多可以消耗3molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、地沟油,塑化剂(邻苯二甲酸酯类物质)均属于高分子化合物都对健康有害 |
| B、家用84消毒液可与清洁剂(主要是盐酸的溶液)混合使用,增强去污能力 |
| C、面粉厂、水泥厂常用静电除尘装置是根据胶体带电这一性质设计的 |
| D、酸雨形成主要来源于SO2或NOx排放所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:
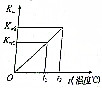 水的离子积常数Kw与温度t(℃)的关系如图所示:
水的离子积常数Kw与温度t(℃)的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤⑦⑨ |
| B、①②④⑤⑦ |
| C、③⑤⑥⑦⑧ |
| D、②④⑥⑦⑨ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com