
【题目】形形色色的物质,构成了我们这个五彩缤纷的世界。世上万物,神奇莫测,常常超乎人们按“常理”的想象。学习物质结构和性质的知识,能使你想象的翅膀变得更加有力。
(1)基态Ga原子的电子排布式是[Ar] __。氮化镓是一种新型材料,可把手机信号放大10倍,氮化镓的功效与电子跃迁有关,而元素的光谱也与电子的跃迁有关。下列变化过程不会产生原子光谱的是__(填字母序号)。
A.[Ar]3d44s2→[Ar]3d54s1
B.![]()
C.![]()
D.![]()
(2)锂离子电池是现代高性能电池的代表,LiFePO4因具有良好的结构稳定性而成为新一代正极材料,这与PO43-的结构密切相关,PO43-的立体构型为___,P、O、S的第一电离能从大到小的顺序为___。
(3)在硫酸铜溶液中加入过量KCN,可生成配位化合物离子[Cu(CN)4]2-,则1mol[Cu(CN)4]2-中含有的σ键的数目为___;写出一种与CN-互为等电子体的单质的分子式___。
(4)钙和钴都是第四周期元素,且原子的最外层电子数相同,钴的熔沸点远高于钙,其原因是___。
(5)Na2S的晶胞结构如图所示。已知Na+的半径为0.102nm,S2-的半径为0.184nm,则Na2S的晶胞参数a=___cm(列出计算式即可)。
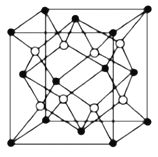
【答案】3d104s24p1 C 正四面体形 O>P>S 8NA N2 钙和钴都属于金属晶体,Ca的原子半径较大且价电子数较少,金属键较弱 ![]() ×10-8
×10-8
【解析】
(1)Ga是31号元素,其基态原子的核外电子排布式为[Ar]3d104s24p1;
A.[Ar]3d44s2→[Ar]3d54s1过程中,前者能量高于后者,发生电子的跃迁,能够产生原子光谱,A不选;
B.![]() 过程中,前者能量低于后者,发生电子的跃迁,能够产生原子光谱,B不选;
过程中,前者能量低于后者,发生电子的跃迁,能够产生原子光谱,B不选;
C.![]() 过程中,前后都为基态原子,没有能量变化,不能够产生原子光谱,C选;
过程中,前后都为基态原子,没有能量变化,不能够产生原子光谱,C选;
D.![]() 过程中,前者能量低于后者,发生电子的跃迁,能够产生原子光谱,D不选;
过程中,前者能量低于后者,发生电子的跃迁,能够产生原子光谱,D不选;
故答案为:3d104s24p1;C;
(2)PO43-中心P原子的价层电子对数为![]() ,不含有孤对电子,则其立体构型为正四面体形;同周期从左到右元素的第一电离能呈增大趋势,同主族从上到下元素的第一电离能逐渐减小,又P原子的3p轨道为3p3半充满结构,其第一电离能比S大,因此第一电离能由大到小的顺序为O>P>S,故答案为:正四面体形;O>P>S;
,不含有孤对电子,则其立体构型为正四面体形;同周期从左到右元素的第一电离能呈增大趋势,同主族从上到下元素的第一电离能逐渐减小,又P原子的3p轨道为3p3半充满结构,其第一电离能比S大,因此第一电离能由大到小的顺序为O>P>S,故答案为:正四面体形;O>P>S;
(3)[Cu(CN)4]2-中Cu2+和CN-形成4个配位键,配位键属于σ键,CN-中C和N形成1个σ键,则1mol[Cu(CN)4]2-中含有的σ键的数目为8NA,原子总数和价电子总数分别都相等的互为等电子体,与CN-互为等电子体的单质可以是N2,故答案为:8NA;N2;
(4)Ca和Co均为金属晶体,Ca的原子半径大于Co,且价电子数比Co少,则Ca的金属键较弱,熔点比Co低,故答案为:钙和钴都属于金属晶体,Ca的原子半径较大且价电子数较少,金属键较弱;
(5)Na2S的晶胞结构中,晶胞参数为a,则体对角线为![]() a,体对角线上黑球与白球间的距离为体对角线长度的
a,体对角线上黑球与白球间的距离为体对角线长度的![]() ,从而得出
,从而得出![]() ×
×![]() a=(0.102+0.184)nm,
a=(0.102+0.184)nm,![]() ,故答案为:
,故答案为:![]() ×10-8。
×10-8。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】恒温条件下,在CH3COONa稀溶液中分别加入少量下列物质:
①固体NaOH;②固体KOH;③固体NaHSO4;④固体CH3COONa;⑤冰醋酸
其中一定可使c(CH3COO-)/c(Na+)比值增大的是 ( )
A. ①② B. ②⑤ C. ①⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列叙述不正确的是( )
![]()
A.化合物(ZXY)2中Z元素的化合价为-2价
B.Y的氧化物对应的水化物可能是弱酸
C.(ZXY)2分子中X原子的杂化方式为sp杂化
D.X、Y、Z、W四种元素电负性的大小顺序为:Z>Y>X>W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3、和FeO)得到绿矾(FeSO4·7H2O),在通过绿矾制备铁黄[FeO(OH)]的流程如下:
![]()
已知:FeS2和铁黄均难溶于水
下列说法不正确的是
A. 步骤①,最好用硫酸来溶解烧渣
B. 步骤②,涉及的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+
C. 步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D. 步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中,只含有下表中所示的四种离子,试推测X离子及其个数b可能为:( )
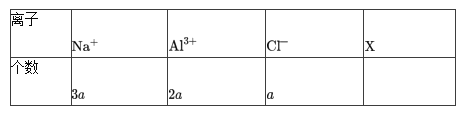
A.SO42- 8aB.OH- 8aC.NO3- 4aD.SO42- 4a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的化工原料,可发生如下转化。下列说法中不正确的是( )
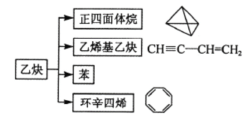
A.以上转化均为加成反应
B.正四面体烷的二氯代物只有1种结构
C.苯乙烯(![]() )和环辛四烯互为同分异构体
)和环辛四烯互为同分异构体
D.等质量的苯和乙烯基乙炔充分燃烧时消耗氧气的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置图的叙述中,正确的是

① ②
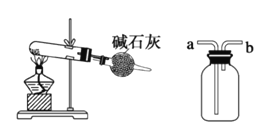
③ ④
A. 装置①:常用于分离互不相溶的液体混合物
B. 装置②:可用于吸收氯化氢、氨气等气体尾气,防止倒吸
C. 装置③:可用于实验室以氯化铵为原料制备少量NH3的实验
D. 装置④:先装满水,再从b口进NO气体,可收集NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如图反应。(图中有些反应的产物和反应条件没有标出)
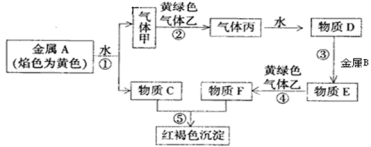
请回答下列问题:
(1)丙的化学式为____。
(2)A的一种氧化物为淡黄色固体,该物质的电子式为___。
(3)写出气体乙与C溶液反应的离子方程式:____。
(4)若将C溶液与E溶液混合,则可以观察到的现象是:____。
(5)配制F溶液时,要将F固体先溶于较浓的盐酸中,再加水稀释,其目的是___(用简单文字和离子方程式说明)。
(6)设计一种检验物质E溶液中金属阳离子实验方案:____(写出实验步骤,现象和结论)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,电解质溶液中的下列关系式不正确的是( )
A.0.1molL-1 CH3COOH溶液加水稀释,n(H+)增大
B.在0.1molL-1的氨水中滴加0.1molL-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=10-amolL﹣1
C.将cmolL-1的醋酸溶液与0.02molL-1NaOH溶液等体积混合后溶液恰好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=![]()
D.已知A-+H2B(过量)═HA+HB-,则结合H+的能力:A-<HB-<B2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com