
【题目】用碳化铝制取甲烷的化学方程式为:Al4C3+12H2O=4Al(OH)3↓+3CH4↑。下列有关化学用语表示正确的是( )
A.铝离子的电子排布式:1s22s22p63s23p1
B.水分子的结构式:H—O—H
C.甲烷的比例模型:![]()
D.氢氧化铝的电离方程式:H++AlO2-+H2O=Al(OH)3=Al3++3OH-
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用化学方程式表示:盐碱地产生碱性的原因:________________________________________________;农业上用石膏降低其碱性的反应原理:_____________________________________。
(2)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m________n (填“>”“<”或“=”)。
(3)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=__________。
(4)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。
①在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+被氧化为Fe3+,下列物质最好采用的是__________。
A.KMnO4 B.H2O2 C.氯水 D.HNO3
②然后再加入适当物质调整溶液至pH=4,使Fe3+转化为Fe(OH)3,调整溶液pH可选用下列物质中的__________。
A.NaOH B.NH3·H2O C.CuO D.Cu(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向50 mL饱和CuCl溶液中缓慢加入NaI固体并搅拌,溶液中c(I-)与c(Cu+)的变化曲线如图所示,已知:Ksp(CuI)=1.0×10-12,下列说法正确的是
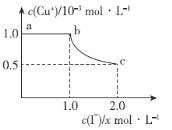
A.Ksp(CuCl)=1.0×10-9
B.图示中的x为10-6
C.向CuI饱和溶液中加入淀粉会出现蓝色
D.曲线bc段内,c(Cl-):c(I-)=106
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的X、Y气体充入一个密闭容器中,一定条件下发生反应并达到平衡:X(g)+Y(g) ![]() 2Z(g) ΔH<0。改变条件达到新平衡后,下列正确的是( )
2Z(g) ΔH<0。改变条件达到新平衡后,下列正确的是( )
A. 升高温度,X的体积分数减小
B. 增大压强(缩小容器体积),Z的浓度不变
C. 保持容器体积不变,充入一定量的惰性气体,Y的浓度不变
D. 保持容器体积不变,充入一定量的Z,X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是( )
A.MnO2与浓盐酸反应制Cl2:MnO2+4HCl![]() Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O =Al(OH)3↓+3H+
C.Na2O2溶于水产生O2:Na2O2+H2O =2Na++2OH-+O2↑
D.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-= CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用下列化学反应在实验室中制备氯气,并进行有关氯气性质的研究。
![]()
(1)该小组同学欲用图所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。
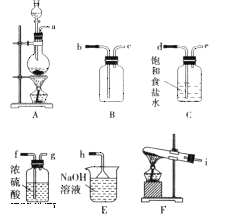
① 应该选择的仪器是__________(填字母)。
② 将各仪器按先后顺序连接起来,应该是a接__________,__________接__________,__________接__________,__________接h(用导管口处的字母表示)。
③ 浓盐酸与二氧化锰反应的离子方程式为__________。
(2)该小组同学设计分别利用图所示装置探究氯气的氧化性。
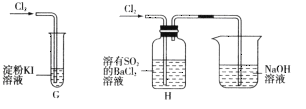
①G中的现象是__________,原因是__________(用化学方程式表示)。
②H中的现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)可以除去工业污水中的氰化物,反应的离子方程式为:2ClO2+2CN-=2CO2↑+N2↑+2Cl-
完成下列填空:
(1)上述反应所涉及元素的原子半径由大到小的顺序是___;其中原子核外有两个未成对电子的元素有___。请比较碳和氮元素非金属性强弱___(用一个化学反应方程式表示)。
(2)二氧化氯还可以除去污水中的锰离子,请配平如下反应:___。
ClO2+MnSO4+H2O→MnO2↓+HCl+H2SO4
若反应中生成0.2molMnO2,则电子转移___个。
(3)氯的另一种氧化物Cl2O每个原子都达到8电子稳定结构,它的电子式为___。
(4)另一种处理含氰化物污水的方法是电解法,分析判断CN-是在___极上(选填编号:①阴;②阳)被反应成CO2和N2,判断的依据是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种粒子。其中N2、ClO-的物质的量随时间变化的曲线如图所示。下列判断不正确的是
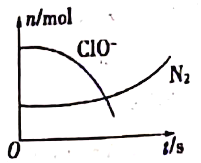
A. 该反应的氧化剂是ClO-
B. 消耗1mol还原剂,转移3mol电子
C. 氧化剂与还原剂的物质的量之比为2:3
D. 该离子方程式为3ClO-+2NH4+=2H++N2↑+3Cl-+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是地壳中含量最多的金属元素,在自然界主要以化合态形式存在于氧化铝中,铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质,冶炼金属铝很重要的一个过程是Al2O3的提纯。工业流程如下:
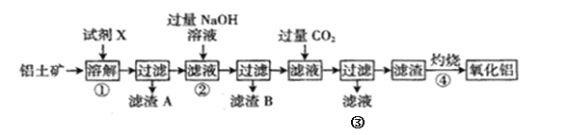
(1)试剂X应选择______(填标号)。
A.过量NaOH溶液 B.过量稀盐酸 C.过量FeCl3溶液
(2)若在实验室进行过滤操作,必须用到的玻璃仪器除了烧杯,还有_________;
(3)滤渣A和B的主要成份分别为_____、______;
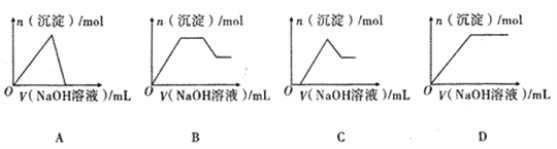
(4)若②中逐滴滴加NaOH溶液,则实验过程中产生沉淀的物质的量与加入NaOH溶液的体积之间的关系图正确的是_______;(填标号)
(5)③中与NaOH溶液反应的离子方程式为__________;
(6)④中发生反应的化学方程式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com