
(1) 甲烷的分子个数为1.204×1023,则甲烷的物质的量为 mol,所含的原子个数共有 个,与这些甲烷质量相等的O2的物质的量为 mol。
(2)含有相同氧原子数目的NO和CO2两种气体,其质量比 ,物质的量比为 ,在标准状态下,体积比为 。
(3)一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol/L的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05mol。
①原NaOH溶液的质量分数为 。
②所得溶液中Cl-的物质的量为 mol。
③所用氯气和参加反应的氢气的物质的量之比n(Cl2)∶n(H2)= 。
(1)0.2 ; NA或6.02×1023; 0.1(1+1+1=3分)
(2)15︰11; 2︰1; 2︰1 (1+1+1=3分)
(3)①10.71% (2分) ②0.25 mol (2分) ③3︰2(2分)
解析试题分析:(1)n=N/NA=1.204×1023/6.02×1023=0.2mol;N=0.2×5NA=NA;n(O2)=0.2×16÷32=0.1mol
(2)15︰11; 2︰1; 2︰1
(3)该过程发生两个反应为HCl+NaOH=NaCl+H2O,Cl2+2NaOH=NaCl+NaClO+H2O。
①原NaOH溶液的质量分数w="0.1L×3.00" mol/L×40g/mol÷(100 mL×1.12g/mL)=10.71%
②根据钠原子守恒知n(Cl-)=n(NaOH)-n(NaClO)=0.3-0.05=0.25mol
③剩余氯气的量为n(Cl2)=n(NaClO)=0.05mol,
反应生成的n(HCl)=n(Cl-)-n(Cl2)反应=0.25-0.05=0.2mol
反应的氯气和氢气的量为n(Cl2)=n(H2)=n(HCl)/2=0.2÷2=0.1mol
所用氯气和参加反应的氢气的物质的量之比n(Cl2)∶n(H2)=(0.1+0.05)∶0.1=3︰2
考点:考查化学计算中物质的量基本计算、浓度的互换、根据方程式计算等有关问题。


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:单选题
设NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.11gT2O含有的中子数为6NA |
| B.1molNa2O2与CO2完全反应转移的电子数为2NA |
| C.常温下,0.2L0.5mol/LNH4NO3溶液的氮原子数小于0.2NA |
| D.标准状况下,2.24LH2S全部溶于水所得溶液中HS-和S2-离子数之和为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列化学用语的理解正确的是
A.离子结构示意图 :可以表示35Cl-,也可以表示37Cl- :可以表示35Cl-,也可以表示37Cl- |
B.电子式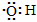 :可以表示羟基,也可以表示氢氧根离子 :可以表示羟基,也可以表示氢氧根离子 |
C.比例模型 :可以表示甲烷分子,也可以表示四氯化碳分子 :可以表示甲烷分子,也可以表示四氯化碳分子 |
D.聚丙烯的结构简式: |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1 g 样品加热,其质量变为w2 g ,则该样品的纯度(质量分数)是( )
A.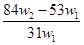 | B.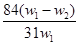 | C.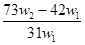 | D.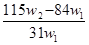 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将amol小苏打和bmol过氧化钠置于某体积可变的密闭容器中充分加热,反应后测得容器内的氧气为1 mol,下列说法一定正确的是
| A.b=2 |
| B.容器中一定没有残余的CO2和水蒸气 |
| C.a:b≥1 |
| D.反应中转移的电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将a g二氧化锰粉末加入b mol/L的浓盐酸c L中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,下列叙述正确的是
A.可以收集到氯气 L L |
B.反应后溶液中的Cl―数目为: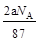 |
C.NA可表示为: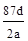 |
D.反应后溶液中的H+数目为: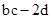 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.在反应KIO3 + 6 HI=KI + 3I2+3 H2O中,每生成3mo1 I2转移的电子数为5NA |
| B.100mL 18.4mo1·L-1硫酸与足量Cu反应,生成SO2的分子数为0.92NA |
| C.1L 0.1 moI·L-1的CH3COOH溶液中所含的离子和分子总数为0.1NA |
| D.将0.lmol FeC13滴人沸水中可制得0.1NA Fe(OH)3胶粒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com