
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2010?����һģ���������й��ס���Ч���Ͷ���ɱ�����������ǽ��չ�����ƣ�
��2010?����һģ���������й��ס���Ч���Ͷ���ɱ�����������ǽ��չ�����ƣ�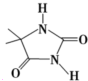

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 2n-7 |
| 2n+1 |
| 2n-7 |
| 2n+1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ������2010�������ѧ������飨һ�� ���ͣ������
�������й��ס���Ч���Ͷ���ɱ�����������ǽ��չ�����ơ�
��1��Cl2��H2O2��ClO2(��ԭ����ΪCl������O3(1molO3ת��Ϊ 1molO2��1molH2O�������ʳ��������������������ʵ�����������������Ч����ߵ��� ��������ţ�
A��Cl2��������B��H2O2�������� C��ClO2�������� D��O3
��2���Ȱ�(NH2Cl������Ϊɱ���������û�ѧ����ʽ��ʾ�Ȱ���ˮ�е�ɱ��������
��
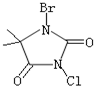
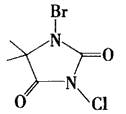
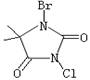 ��3�����庣��C5H6BrClN2O2����һ�ֱȽϰ�ȫ�����������Ƽ��������Ʒ����ṹʽ����ͼ��ʾ��
��3�����庣��C5H6BrClN2O2����һ�ֱȽϰ�ȫ�����������Ƽ��������Ʒ����ṹʽ����ͼ��ʾ��
���庣����ˮ�е�ˮ����̱Ƚϸ��ӣ���Ҫ��ˮ�����ɴ�±��
�ͺ����뻭������Ľṹʽ��
��
��4���Բ�(Pt������Ϊ�缫����KOH��ҺΪ���Һ,�õ�ⷨ���Ʊ��������(K2FeO4����
д�������ĵ缫��Ӧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ר���� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������й��ס���Ч���Ͷ���ɱ�����������ǽ��չ�����ơ�
��1��Cl2��H2O2��ClO2(��ԭ����ΪCl������O3(1molO3ת��Ϊ 1molO2��1molH2O�������ʳ��������������������ʵ�����������������Ч����ߵ��� ��������ţ�
A��Cl2��������B��H2O2�������� C��ClO2�������� D��O3
��2���Ȱ�(NH2Cl������Ϊɱ���������û�ѧ����ʽ��ʾ�Ȱ���ˮ�е�ɱ��������
��
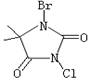 ��3�����庣��C5H6BrClN2O2����һ�ֱȽϰ�ȫ�����������Ƽ��������Ʒ����ṹʽ����ͼ��ʾ��
��3�����庣��C5H6BrClN2O2����һ�ֱȽϰ�ȫ�����������Ƽ��������Ʒ����ṹʽ����ͼ��ʾ��
���庣����ˮ�е�ˮ����̱Ƚϸ��ӣ���Ҫ��ˮ�����ɴ�±��
�ͺ����뻭������Ľṹʽ��
��
��4���Բ�(Pt������Ϊ�缫����KOH��ҺΪ���Һ,�õ�ⷨ���Ʊ��������(K2FeO4����
д�������ĵ缫��Ӧʽ�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com