
已知:pOH=-lg c(OH-),在常温下溶液中的pH+pOH=14,又已知正常人(人的体温高于室温)的血液pH=7.3,则正常人血液的pOH是
A.大于6.7 B.小于6.7
C.等于6.7 D.无法判断
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
已知可逆反应:A(g)+B(g)  C(g)+D(g) ΔH<0。请回答下列问题:
C(g)+D(g) ΔH<0。请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(A)=1 mol·L-1,c(B)=2.4 mol·L-1,达到平衡时,A的转化率为60%,此时B的转化率为________ _______________________________。
_______________________________。
(2)若反应温度降低,则B的转化率将________(填“增大”、“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为c(A)=4 mol·L-1,c(B)=a mol·L-1,达到平衡后c(C)=2 mol·L-1,则a=________。
(4)若反应温度不变,反应物的起始浓度分别为c(A)=c(B)=b mol·L-1,达到平衡后c(D)=________。(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
某探究小组在实验室中用铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)提取氧化铝。回答下列问题:

(1)在实验中需用1 mol/L的NaOH溶液480 mL,配制该溶液已有下列仪器:托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是________________。在灼烧操作中用到下列仪器中的一种,其名称是________________。
(2)写出步骤①中发生反应的离子方程式
________________________________________________________________________。
(3)操作③中洗涤如何操作______________________________________.
 (4)甲同学在实验室中用如图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象。
(4)甲同学在实验室中用如图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象。
乙同学分析认为:甲同学通入CO2的量不足是导致实验失败的原因之一,你认为乙的分析是否合理?______________________。若合理,请用离子方程式解释其原因________________________。(若你认为不合理,该空不作答)
丙同学分析认为:甲同学通入的CO2中含有HCl气体,也是导致实验失败的原因,在实验中增加某装置可解决这个问题。请帮助丙同学画出该装置图,并注明试剂名称。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)利用SiO2的化学性质,写出实现下列变化的化学方程式。
SiO2 → 硅酸
SiO2 →高纯度的硅
(2)实验室中盛放强碱(氢氧化钠)溶液的玻璃试剂瓶不能用玻璃塞,试说明原因:
查看答案和解析>>
科目:高中化学 来源: 题型:
在25 ℃时,向V mL pH=m的HNO3中滴加pH=n的KOH溶液10V mL时,溶液中NO 的物质的量恰好等于加入的
的物质的量恰好等于加入的 K+的物质的量,则m+n的值为
K+的物质的量,则m+n的值为
A.13 B.14
C.15 D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)水的电离平衡曲线如图所示,若A点表示25 ℃时水的电离达平衡时的离子浓度,B点表示100 ℃时水的电离达平衡时的离子浓度。则100 ℃时1 mol·L-1的NaOH溶液中,由水电离出的c(H+)________ mol·L-1,KW(25℃)________KW(100 ℃)(填“>”、“<”或“=”)。25 ℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是________(填“促进”、“抑制”或“不影响”)。
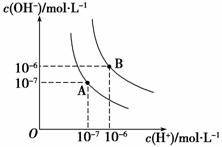
(2)电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
| 化学式 | 电离平衡常数(25 ℃) |
| HCN | K=4.9×10-10 mol·L-1 |
| CH3COOH | K=1.8×10-5 mol·L-1 |
| H2CO3 | K1=4.3×10-7 mol·L-1、 |
| K2=5.6×10-11 mol·L-1 |
①25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为__________________________________________________________________。
②25 ℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液显碱性,则
c(Na+)________________________________________________________________________
c(CH3COO-)(填“>”、“<”或“=”)。
③向NaCN溶液中通入少量CO2,所发生反应的化学方程式为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对实验Ⅰ~Ⅳ的实验现象预测正确的是( )
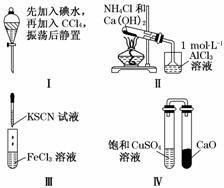
A.实验Ⅰ:液体分层,下层呈无色
B.实验Ⅱ:烧杯中先出现白色沉淀,后溶解
C.实验Ⅲ:试管中溶液颜色变为红色
D.实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4.3×10-7 |
| K2=5.6×10-11 |
A.c(HCO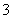 )>c(ClO-)>c(OH-)
)>c(ClO-)>c(OH-)
B.c(ClO-)>c(HCO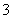 )>c(H+)
)>c(H+)
C.c(HClO)+c(ClO-)=c(HCO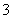 )+c(H2CO3)
)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO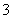 )+c(ClO-)+c(OH-)
)+c(ClO-)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com