
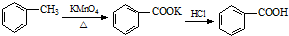
| 名称 | 性状 | 熔点 (℃) | 沸点 (℃) | 密度 (g/mL) | 溶解度(g) | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.4[1] | 248 | 1.2659 | 微溶[2] | 易溶 |
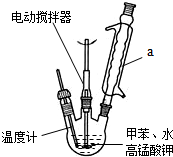 装置a的作用是
装置a的作用是 +
+ +
+ +2KMnO4
+2KMnO4| 加热 |
 +2MnO2↓+H2O+KOH;
+2MnO2↓+H2O+KOH;| 100ml |
| 25ml |
| 1.1712g |
| 1.22g |


科目:高中化学 来源: 题型:
| NaOH溶液起始读数 | NaOH溶液终点读数 | |
| 第一次 | 0.01mL | 18.20mL |
| 第二次 | 0.20mL | 18.41mL |
| 第三次 | 0.40mL | 18.60mL |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
 铁及其化合物应用广泛,例如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等.
铁及其化合物应用广泛,例如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、气体A为SO2和H2的混合物 |
| B、气体A中SO2和H2的体积比为4:1 |
| C、反应中共消耗锌97.5 g |
| D、反应中共转移电子1.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
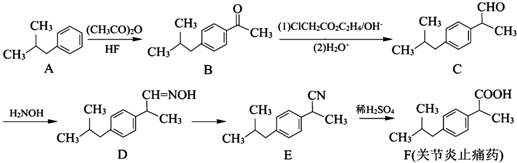
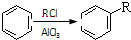 ②
②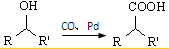 (R、R′表示烃基)
(R、R′表示烃基)| HBr |
| NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com