
【题目】用金属钴板(含少量Fe、Ni)制备应用广泛的氯化钴的工艺流程如下:
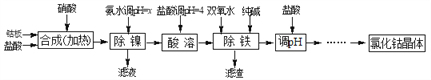
注:钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。
有关钴、镍和铁化合物的性质见下表:
化学式 | 沉淀完全时的pH | 钴镍性质 |
Co(OH)2 | 9.4 | Co+2HCl=CoCl2+H2↑ Co2++2NH3·H2O=Co(OH)2↓+2NH4+ Co2++2H2O Ni+2HCl=NiCl2+H2↑ Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O |
Fe(OH)2 | 9.6 | |
Fe (OH)3 | 3.7 |
(1)“除镍”步骤中,NH3·H2O用量对反应收率的影响见表中数据:从表中数据可知,当PH调节至x=_______时,除镍效果最好。
加NH3·H2O调pH | 收率/% | Ni2+含量/% |
9 | 98.1 | 0.08 |
9.5 | 98 | 0.05 |
10 | 97.6 | 0.005 |
10.3 | 94 | 0.005 |
(2)“除镍”步骤必须控制在一定的时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为________________。
(3)“除铁”步骤中加入双氧水发生反应的离子方程式是________________________。
(4)“除铁”步骤中加入的纯碱作用是________________________________。
(5)在“调pH”步骤中,加盐酸的作用是______________________________。
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O![]() Fe(OH)3+3H+的平衡常数为_____________________。
Fe(OH)3+3H+的平衡常数为_____________________。
【答案】 10 4Co(OH)2+O2+2H2O=4Co(OH)3 (没有配平扣1分) 2Fe2++H2O2+2H+=2Fe3++2H2O (没有配平扣1分) 使Fe3+转化为Fe(OH)3沉淀而除去(或2Fe3++3CO32-+6H2O=2Fe(OH)3↓+3CO2↑) 防止Co2+水解 2.5×10-5 (mol·L-1)2(没有单位不扣分)
【解析】用金属钴板(含少量Fe、Ni)制备应用广泛的氯化钴的工艺流程为:钴板在稀硝酸作催化剂条件下反应生成氯化镍、氯化钴和氯化铁、氯化亚铁等,调节溶液的pH除去镍,然后加入双氧水将亚铁离子氧化成铁离子,然后加入纯碱将铁离子转化成氢氧化铁除去,最后经过一系列操作得到氯化钴晶体。
(1)根据表中的数据知道,当pH等于10的时,收率最高,镍离子的含量最小,除镍效果最好,故答案为:10;
(2)钴离子易从正二价容易被氧气氧化到正三价,发生的化学方程式为:4Co(OH)2+O2+2H2O=4Co(OH)3,故答案为:4Co(OH)2+O2+2H2O=4Co(OH)3;
(3)双氧水具有氧化性,可以将亚铁离子氧化为正三价,发生的化学反应为:2Fe2++H2O2+2H+=2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(4)加入碳酸钠可以和酸发生反应,在适当的环境下,可以让铁离子形成沉淀而除去,所以加入的纯碱作用是起到调节溶液的pH的作用,故答案为:使铁离子转化为氢氧化铁沉淀而除去(或2Fe3++3CO32-+6H2O=2Fe(OH)3↓+3CO2↑);
(5)钴离子是弱碱阳离子,能发生水解,显示酸性,加入盐酸可以防止Co2+水解,故答案为:防止Co2+水解;
(6)Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-)=4.0×10-38,c(H+)=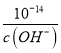 ,反应Fe3++3H2OFe(OH)3+3H+的平衡常数K=
,反应Fe3++3H2OFe(OH)3+3H+的平衡常数K= =
=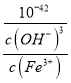 =
=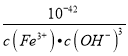 =
=![]() =2.5×10-5,故答案为:2.5×10-5。
=2.5×10-5,故答案为:2.5×10-5。


科目:高中化学 来源: 题型:
【题目】某同学查阅教材得知,普通锌锰电池筒内无机物的主要成分为MnO2、NH4C1、ZnCl2等。他在探究废干电池内的黑色固体回收利用时,进行如图所示实验。下列有关实验的叙述不正确的是
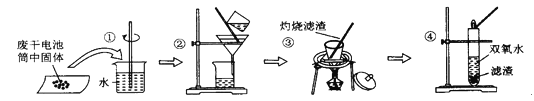
A. 操作①中玻璃棒能加快固体溶解
B. 操作②为过滤,得到的滤液显酸性
C. 操作③盛放药品的仪器是坩埚
D. 操作④的目的是除去滤渣中的杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是 ( )
A. 纯碱溶于热水后去污效果增强,说明纯碱的水解反应是吸热反应
B. NH3(g) + HCl(g) = NH4Cl(s) 在较低温度下能自发进行,说明该反应的ΔH>0
C. 500℃、30 MPa下,将7 g N2和3 g H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
D. 甲烷的燃烧热(ΔH)为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)= CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
【答案】A
【解析】A. 纯碱溶于热水后去污效果增强,说明升高温度促进了水解,使水解平衡正向移动,所以可以说明纯碱的水解是吸热反应,故A正确;B. 根据△G=△H-T△S可知,当△G小于0时反应自发进行,由于反应NH3(g) + HCl(g) = NH4Cl(s)是熵值减小的反应,所以如果该反应在较低温度下能自发进行,则说明该反应的△H<0,故B错误;C.因合成氨的反应是可逆反应,所以无法确定将7 g N2和3 g H2置于密闭容器中充分反应后,生成了多少NH3(g),故无法计算该反应的焓变,故C错误;D. 燃烧热指的是1mol纯物质完全燃烧生成稳定的氧化物时所放出的能量,所以生成的水应为液态,即甲烷燃烧的热化学方程式应表示为CH4(g)+2O2(g)= CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1,故D错误;答案选A。
【题型】单选题
【结束】
14
【题目】在0.1 mol·L-1的CH3COOH溶液中,要抑制醋酸电离,且c(H+)增大,应采取的措施是
A. 加水 B. 升温 C. 加适量CH3COONa固体 D. 通适量HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有a.BaCl2 b.金刚石 c.NH4Cl d.Na2SO4 e.干冰 f.碘片六种物质,按下列要求回答(若有多个选项的,多选错选不给分):
①熔化时需要破坏共价键的是______, 熔点最高的是_______,熔点最低的是_______。
②属于离子化合物的是________,只含有离子键的物质是________,含有两种化学键的物质是_________,含有分子间作用力的是__________。
(2)看下图回答下列问题
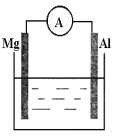
①若烧杯中溶液为稀硫酸,则观察到的现象是___________,负极反应式为___________。
②若烧杯中溶液为氢氧化钠溶液,则负极为_______(填Mg或Al),总反应方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大脑的生长发育与不饱和脂肪酸密切相关,深海鱼油中提取的“DHA”就是一种不饱和程度很高的脂肪酸,称为“脑黄金”,它的分子中含有6个碳碳双键,名称为二十六碳六烯酸,其化学式为
A. C25H50COOH B. C26H41COOH C. C25H39COOH D. C26H47COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取pH=2的两种二元酸H2A与H2B各1mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述正确的是( )
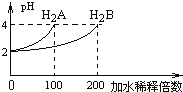
A. H2A为二元弱酸,稀释前c(H2A)=0.005mol/L
B. NaHA水溶液中:c(Na+)+ c(H+)= 2c(A2-)+ c(OH-)
C. 含等物质的量的NaHA、NaHB的混合溶液中:c(Na+)= c(A2-)+ c(B2-)+ c(HB-)+ c(H2B)
D. pH=10的NaHB溶液中,离子浓度大小为:c(Na+)>c(HB-)>c(OH-)>c(B2-)>c(H2B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酸盐是一种常见的食品添加剂,用如下图实验可检验某食品中亚硫酸盐含量(所加试剂均足量)。下列说法不正确的是

A.亚硫酸盐作为食品添加剂,作用是防腐保鲜
B.反应①过程中通入N2的作用是将装置中空气和生成的气体全部赶出
C.测定样品质量及③中耗碱量,可测定样品中亚硫酸盐含量
D.若仅将②中的氧化剂“H2O2溶液”替换为碘水,对测定结果无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.铁是应用最广泛的金属,铁的卤化物、氯化物以及高价铁的含氧酸盐均为重要化合物。已知氧化铁是一种重要的化工原料,无水氯化铁遇潮湿空气极易吸水生成FeCl3·nH2O。
(1)某学习小组用下图装置在实验室制备无水氯化铁,请你一起参与该小组的活动。
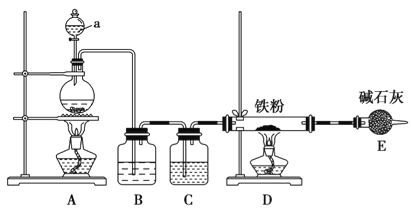
①装置A中发生的离子方程式_______________
②装置B的作用是________,C中的试剂______________。
③实验开始时先点燃___处酒精灯;装置E的作用为__________。
(2)工业上制备无水氯化铁的一种工艺流程如下:
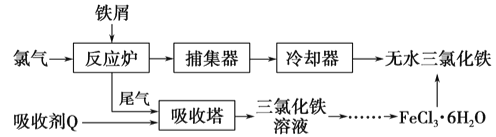
①吸收塔中发生反应的离子方程式为__________
②简述由FeCl3·6H2O晶体得到无水氯化铁的操作:____________
Ⅱ.利用如图所示的装置,可以验证NH3和HCl的有关性质。实验前a、b、c活塞均关闭。
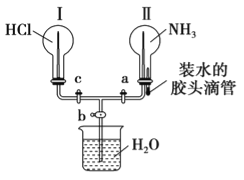
(1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是______。
(2)若先打开a、c活塞,再挤压胶头滴管(假设NH3不能被完全吸收),在烧瓶Ⅱ中可观察到的现象是_____。
(3)通过挤压胶头滴管和控制活塞的开关,要在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙醛的说法错误的是( )
A. 一个乙醛子有6个σ键,1个π键
B. 乙醛分子中存在非极性键
C. 乙醛在催化剂铜存在下可以氧化生成乙醇
D. 乙醛晶体属于分子晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com