
短周期金属元素甲~戊在元素周期表中的相对位置如图所示。下列判断正确的是( )。
甲 | 乙 |
|
丙 | 丁 | 戊 |
A.原子半径:丙<丁<戊 B.金属性:甲>丙
C.氢氧化物碱性:丙>丁>戊 D.最外层电子数:甲>乙
科目:高中化学 来源:2014年化学高考题型专练十六 基本理论综合应用题练习卷(解析版) 题型:填空题
多晶硅是太阳能光伏产业的重要原材料。
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
SiO2(s)+C(s)=SiO(g)+CO(g) ΔH=a kJ·mol-1
2SiO(g)=Si(s)+SiO2(s) ΔH=b kJ·mol-1
①反应SiO2(s)+2C(s)=Si(s)+2CO(g)的ΔH=________ kJ·mol-1(用含a、b的代数式表示)。
②SiO是反应过程中的中间产物。隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式为________________________________。
(2)粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:
SiHCl3(g)+H2(g) Si(s)+3HCl(g)。
Si(s)+3HCl(g)。
不同温度及不同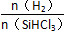 时,反应物X的平衡转化率关系如图所示。
时,反应物X的平衡转化率关系如图所示。
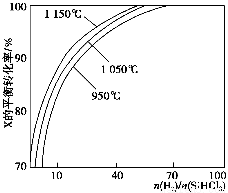
①X是________(填“H2”或“SiHCl3”)。
②上述反应的平衡常数K(1 150 ℃)________K(950 ℃)(填“>”、“<”或“=”)。
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。
①用粗硅作原料,熔融盐电解法制取硅烷原理如图所示,电解时阳极的电极反应式为_________________________________________。
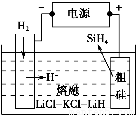
②硅基太阳电池需用N、Si两种元素组成的化合物Y作钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到,已知Y中Si的质量分数为60%,Y的化学式为________。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十 电解质溶液中微粒浓度的关系练习卷(解析版) 题型:选择题
25 ℃时,x mol·L-1氢氟酸水溶液中,加入KOH固体调节溶液的pH(忽略加入固体引起的溶液体积变化),得到c(HF)、c(F-)与溶液pH的变化关系如图所示。下列说法正确的是 ( )。

A.当c(F-)>c(HF)时,溶液呈碱性
B.当pH=2时,c(F-)<c(K+)
C.25 ℃时,氢氟酸的电离平衡常数为4×10-6
D.当pH=5时,c(HF)+c(K+)+c(H+)-c(OH-)=x mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练八 化学反应速率和化学平衡分析与判断练习卷(解析版) 题型:选择题
在密闭容器中进行反应CH4(g)+H2O(g) CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断不正确的是( )。
CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断不正确的是( )。

A.10 min时,改变的外界条件可能是升高温度
B.0~10 min内,v(H2)=0.15 mol·L-1·min-1
C.恒温下,缩小容器体积,一段时间内v(逆)>v(正)
D.12 min时,反应达平衡的本质原因是气体总质量不再变化
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练五 元素周期表中位-构-性关系的分析练习卷(解析版) 题型:选择题
X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F都是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1 mol·L-1 D溶液的pH为13(25 ℃)。它们满足如图转化关系,则下列说法正确的是( )。
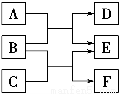
A.原子半径W>Z>Y>X
B.0.1 mol·L-1 F溶液中阴离子总的物质的量大于0.1 mol·L-1 D溶液中阴离子总的物质的量
C.0.1 mol B与足量C完全反应共转移电子数0.1NA
D.Z元素的最高正价为+6
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练二 化学常用计量的理解和综合应用练习卷(解析版) 题型:选择题
阿伏加德常数约为6.02×1023 mol,下列说法中正确的是 ( )。
A.4.2 g丙烯(CH3CH===CH2)和乙烯的混合物中所含的碳原子数为0.3×6.02×1023
B.4.48 L N2O与CO2的混合气体所含电子数为0.2×22×6.02×1023
C.1 mol HCl和NH3的混合气体所含分子数为6.02×1023
D.100 mL 1 mol·L-1醋酸溶液中CH3COO-数目为0.1×6.02×1023
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练三 特定条件下离子方程式的书写与判断练习卷(解析版) 题型:选择题
向等物质的量浓度的NaHCO3和Ca(HCO3)2的混合溶液中,加入一定量NaOH溶液时,不可能发生的离子反应方程式是 ( )。
A.OH-+HCO3—=CO32—+H2O
B.Ca2++OH-+HCO3—=CaCO3↓+H2O
C.Ca2++2OH-+2HCO3—=CaCO3↓+2H2O+CO32—
D.Ca2++3OH-+3HCO3—=CaCO3↓+3H2O+2CO32—
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练一 化学与科学技术社会环境的关系练习卷(解析版) 题型:选择题
2013年4月22日是第44个“世界地球日”,其主题为“珍惜地球资源,转变发展方式”。下列做法符合这一主题的是( )。
①开发太阳能、风能和氢能等能源 ②大量开采地下水,以满足生产、生活的需求 ③在含硫的煤中加入适量生石灰 ④利用苯、甲苯等有机物代替水作溶剂 ⑤利用可降解的“玉米塑料”生产一次性饭盒
A.①②③ B.①③⑤ C.②④⑤ D.①②④
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练9-2电解池金属电化学腐蚀与防护练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀
B.铅蓄电池放电时的负极和充电时的阳极均发生还原反应
C.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al
D.电解食盐水一段时间后,可通入一定量的HCl气体来恢复原溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com