
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
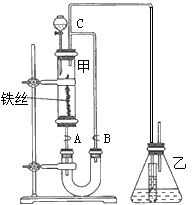
(1)第一步,在分液漏斗中依次加入10 mL苯和5 mL液溴,使之混合均匀,此时观察到溴溶于苯,不反应,溶液呈深棕红色。
第二步,打开分液漏斗活塞,将苯、溴混合液按一定速率逐滴加入玻璃管甲中的铁丝上,观察到的现象是______________________________________________________。
从上述两步观察到的现象差异,可得出的结论是__________________________________。
(2)第三步,几分钟后,打开胶皮管夹A和B,使反应混合液流入U形管中,打开管夹B的原因是________________________________________________;然后通过分液漏斗向U形管中加入适量的NaOH溶液,目的是__________。
(3)第四步,关闭胶皮管A和B,连同A和B一起取下U形管,用力振荡并静置后,观察到溴苯的颜色是__________,它在U形管中液体的______________(填“上”或“下”)层。此步关闭管夹A和B的目的是______________________________________________________。
(4)要证明上述溴跟苯的反应是取代而不是加成反应,请根据装置乙的作用完成下列各题:
①小试管内的液体是__________(填名称),作用是______________________________。
②锥形瓶内的液体是__________(填名称),作用是______________________________。
③反应后,向锥形瓶内滴加试剂__________(填名称)溶液,作用是__________。此外,装置乙还能起到__________的作用。
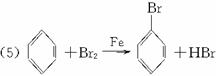
(5)写出上述苯跟溴反应的化学方程式________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014届浙江省高一上学期期中考试化学试卷 题型:实验题
(20分)氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用到氯气。工业上通常采用电解法制氯气:观察下图,回答:
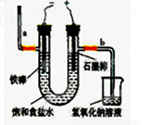
Ⅰ(1)若饱和食盐水中含有酚酞,通电后_____(填a或b)侧先变红。
(2)电解反应的化学方程式为__________________
Ⅱ某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
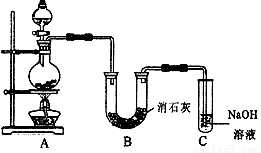
(1) 在A装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,反应化学方程式为 ,若在标准状态下收集到22.4升的氯气,则被氧化的HCl的物质的量是 。
(2) 漂白粉将在U形管中产生,其化学方程式是 。
(3) C装置的作用是 。
(4) 此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是 。
②试判断另一个副反应(用化学方程式表示) 。为避免此副反应的发生,可将装置作何改进 。
(5)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是 。
A.食盐 B.食醋 C.烧碱 D.纯碱
查看答案和解析>>
科目:高中化学 来源: 题型:
用二氧化氯(ClO2)、高铁酸钠(Na2FeO4,摩尔质量为166 g?mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理的新技术。ClO2和Na2FeO4在水处理过程中分别只被还原为Cl-和Fe3+。
(1)如果以单位质量的氧化剂所得到的电子数来表示消毒效率。那么ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是_____>________>__________。
(2)二氧化氯是一种黄绿色有刺激性气味的气体。其熔点为-59℃,沸点为11.0℃,易溶于水。ClO2可以看做是亚氯酸和氯酸的混合酸酐。工业上用湿润的KClO3和草酸在60℃时反应制得。某学生用如下图所示的装置模拟工业制取并收集ClO2,其中A为ClO2的发生装置,B为ClO2的收集装置,C为尾气吸收装置。请问: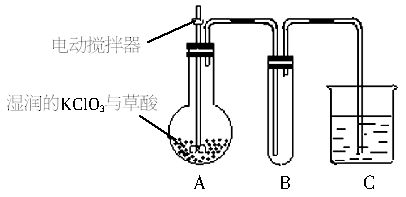
①A部分还应添加温度控制(如水浴加热)装置,B部分还应补充什么装置_________。
②C中应装的试剂为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com