
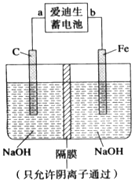
 铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:
铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:分析 (1)钢铁在潮湿的空气中发生吸氧腐蚀,正极上得电子发生还原反应;负极上铁失电子发生氧化反应,正极上得电子发生还原反应,二价铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁被氧化生成氢氧化铁,氢氧化铁失去部分水生成铁锈;铁和铁离子能发生氧化还原反应生成亚铁离子.
(2)①放电时,铁棒作负极,碳棒作正极,据此判断a的电极;失电子的物质发生氧化反应.
②铁失电子和氢氧根离子生成高铁酸根离子和水.
③高铁酸根离子有强氧化性,被还原生成的三价铁离子能发生生成胶体,胶体具有吸附性.
解答 解:(1)钢铁在潮湿的空气中发生吸氧腐蚀,正极上氧气得电子和水反应生成氢氧根离子O2+4e-+2H2O=4OH-;负极上铁失电子发生氧化反应,正极上发生的反应为O2+4e-+2H2O=4OH-,二价铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁被氧化生成氢氧化铁,氢氧化铁失去部分水生成铁锈,所以铁锈的成分是Fe2O3•xH2O;铁和铁离子能发生氧化还原反应生成亚铁离子2Fe3++Fe=3Fe2+,导致溶液中不存在铁离子.
故答案为:O2+4e-+2H2O=4OH-;Fe2O3•xH2O;2Fe3++Fe=3Fe2+.
(2)①放电时,铁作负极,碳棒作正极,所以放电时a是负极,b是正极;充电时,氢氧化镍失电子生成氧化镍,发生氧化反应.
故答案为:a;氧化反应.
②阳极上铁失电子和氢氧根离子反应生成高铁酸根离子和水,离子方程式为:Fe-6e-+8OH-=FeO42-+4H2O.
故答案为:Fe-6e-+8OH-=FeO42-+4H2O.
③高铁酸钠具有强氧化性,所以能杀菌消毒;高铁酸钠能被还原生成铁离子,铁离子能水解生成氢氧化铁胶体,胶体具有吸附性,能吸附悬浮杂质,所以能净水.
故答案为:BC.
点评 本题考查了原电池原电池和电解池原理,题目难度中等,注意把握原电池和电解质中电极的判断方法以及电极方程式的书写方法是解题的关键,侧重于考查学生的分析能力和对基础知识的应用能力.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1013的溶液中:NH4+、Ca2+、Cl-、K+ | |
| B. | Kw/c(OH-)=1.0mol•L-1的溶液中:Mg2+、NO3、NH4+、I- | |
| C. | 中性溶液中:K+、Cl-、Na+、CO32- | |
| D. | 无色溶液中:Fe3+、Cl-、Na+、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| X | Y | |
| Z | W |
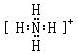 ,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).
,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是( )
用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是( )| ①中实验 | ②中现象 | |
| A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| B | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| C | NaHC03固体受热分解 | 澄済石灰水变浑浊 |
| D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
| A. | 答案A | B. | 答案B | C. | 答案C | D. | 答案D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H12的烃 | B. | 分子式为C4H10O的醇 | ||
| C. | 分子式为C4H8的烯烃 | D. | 分子式为C3H6O2的酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠与二氧化硫反应时可生成硫酸钠 | |
| B. | 1mol过氧化钠中阴离子数目约为6.02×1023 | |
| C. | Na2O2与CO2反应时,Na2O2是氧化剂CO2是还原剂 | |
| D. | 将等物质的量的Na2O和Na2O2分别溶于等质量的足量水中所得溶液的质量相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com