
【题目】下列8种化学符号:168O2、188O2、H、126C、![]() Na、
Na、![]() 7N、146C、
7N、146C、![]() Mg。
Mg。
(1)表示核素的符号共________种。
(2)互为同位素的是______________。
(3)质量相同的H![]() O和D
O和D![]() O所含中子数之比为________。
O所含中子数之比为________。
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2 [Be(OH) 4]的离子方程式__________________。
(5)Be(OH) 2与Mg(OH)2可用_______________试剂鉴别。
【答案】 6 126C 146C 8∶9 Be+2OH-+2H2O====[Be(OH)4]2-+H2↑ NaOH (或氢氧化钠)溶液
【解析】(1)核素指具有一定质子数和一定中子数的一种原子。所以上述中有:H、126C、![]() Na、
Na、![]() 7N、146C、
7N、146C、![]() Mg六种核素。答案:6。
Mg六种核素。答案:6。
(2)同位素是指质子数相同,质量数不同的不同核素。如126C 146C。
(3)H![]() O的中子数为8,D
O的中子数为8,D![]() O的中子数10,质量相同的H
O的中子数10,质量相同的H![]() O和D
O和D![]() O所含中子数之比为m/18
O所含中子数之比为m/18![]() :m/20
:m/20![]() = 8∶9
= 8∶9
(4)根据周期表对角线规则,金属Be与Al单质性质相似,所以Be与NaOH溶液反应也能生成Na2 [Be(OH) 4]和氢气,离子方程式: Be+2OH-+2H2O====[Be(OH)4]2-+H2↑
(5)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似,因为Al(OH)3具有两性,可以和酸和碱反应,所以Be(OH) 2也可以和强碱反应,而Mg(OH)2不能和氢氧化钠反应,所以就可用氢氧化钠溶液鉴别。答案:NaOH (或氢氧化钠)溶液。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】锰酸锂(LiMn2O4)可作为锂离子电池的正极材料.工业上利用软锰矿浆吸收含硫烟气(SO2 和O2)制备锰酸锂,生产流程如图1: 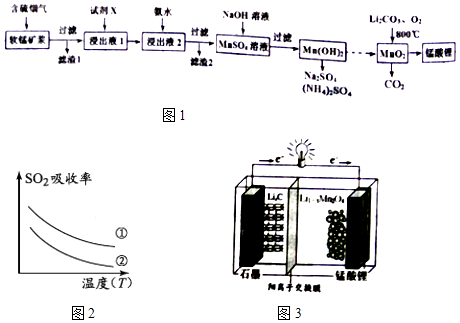
已知:①软锰矿主要成分为MnO2 , 含少量Fe2O3、FeO、Al2O3、SiO2等杂质.
②软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强.
③部分氢氧化物沉淀相关的溶液pH如表一:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
(1)已知:(图2)表二 表二
实验序号 | SO2浓度(gm﹣3) | 烟气流速(mLmin﹣1) |
① | 4.1 | 55 |
② | 4.1 | 96 |
下列措施可提高SO2吸收率的是(填序号)
a.降低通入含硫烟气的温度 b.升高通入含硫烟气的温度
c.减少软锰矿浆的进入量 d.减小通入含硫烟气的流速
(2)加入试剂X能提高产品纯度,则X可以是(填化学式)
(3)加氨水调溶液pH在5~6之间,目的是 .
(4)锰酸锂可充电电池(图3)的总反应式为:Li1﹣xMnO4+LixC ![]() LiMnO4+C(x<1) ①放电时,电池的正极反应式为
LiMnO4+C(x<1) ①放电时,电池的正极反应式为
②充电时,若转移1mole﹣ , 则石墨电极将增重g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ni2O3主要用作陶瓷、搪瓷和玻璃的着色剂,也可用于镍粉的制造.以镍粉废料为原料制备Ni2O3的工艺如图1 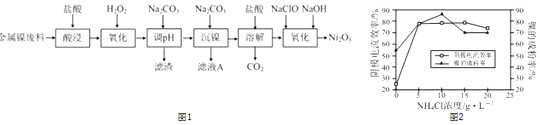
回答下列问题:
(1)Ni2O3中Ni的化合价为 .
(2)提高“酸浸”、“酸溶”速率时,温度不宜过高,其原因是 .
(3)加入H2O2“氧化”的离子方程式为;滤渣A的主要成分是(填化学式).
(4)工艺中分步加入Na2CO3的作用是;为提高原料的利用率,应控制加入NaClO与NaOH的物质的量之比为 .
(5)工业上,用镍为阳极,电解0.1mol/L NiCl2溶液与一定量NH4Cl组成的混合溶液,可得高纯度的球形超细镍粉.当其他条件一定时,NH4Cl的浓度对阴极电流效率(电流效率是指电解时,在电极上实际沉积的物质的量与理论析出量之比)及镍的成粉率的影响如图2所示: ①为获得高纯度的球形超细镍粉,NH4Cl溶液的浓度最好控制为mol/L.
②当NH4Cl溶液的浓度大于15g/L时,阴极有气体生成,导致阴极电流效率降低,请结合平衡移动原理解释其原因: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生如下反应:mA(g)+nB(g)pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的 ![]() ,当达到新平衡时,C的浓度为原来的1.9倍,下列说法正确的是( )
,当达到新平衡时,C的浓度为原来的1.9倍,下列说法正确的是( )
A.m+n>p
B.平衡向逆反应方向移动
C.A的转化率提高
D.C的体积分数增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时水的离子积常数为KW . 该温度下,将浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.a=b
B.混合溶液中,c(H+)= ![]() ?mol/L
?mol/L
C.混合溶液的pH=7
D.混合溶液中,c(H+)+c(B+)=c(OH﹣)+c(A﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的两种一元酸x和y,体积均为100mL,稀释过程中pH与溶液体积的关系如图所示.分别滴加NaOH溶液(c=0.1mol/L)至pH=7,消耗NaOH溶液的体积为Vx、Vy , 则( ) 
A.x为弱酸,Vx<Vy
B.x为强酸,Vx>Vy
C.y为弱酸,Vx<Vy
D.y为强酸,Vx>Vy
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关纸层析法实验的说法正确的是( )
A.滤纸作为固定相,滤纸上吸附的水作为流动相
B.滤纸作为惰性支持物,滤纸上吸附的水作为流动相
C.滤纸上吸附的水作为固定相,溶于水的有机溶剂作为流动相
D.滤纸上吸附的水作为流动相,不溶于水的有机溶剂作为固定相
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用硫酸酸化的草酸(H2C2O4 , 二元弱酸)溶液能将KMnO4溶液中的MnO4﹣转化为Mn2+ . 某化学小组研究发现,少量MnSO4可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,请完成以下实验设计表.
实验 | 温度 | 初始pH | 0.1mol/L | 0.01mol/L | 蒸馏水 | 待测数据(反应混合液褪色 |
① | 常温 | 1 | 20 | 50 | 30 | t1 |
② | 常温 | 2 | 20 | 50 | 30 | t2 |
③ | 常温 | 2 | 40 | a | b | t3 |
表中a、b的值分别为:a=、b=
(2)该反应的离子方程式 .
(3)若t1<t2 , 则根据实验①和②得到的结论是
(4)请你设计实验④验证MnSO4对该反应起催化作用,完成表中内容.
实验方案(不要求写出具体操作过程) | 预期实验结果和结论 |
若反应混合液褪色时间小于实验①中的t1 , 则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
(5)某化学小组用滴定法测定KMnO4溶液物质的量浓度:取W g草酸晶体(H2C2O42H2O,其摩尔质量126g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定两次,平均消耗KMnO4溶液
V mL.请回答下列问题:
①该测定方法中(填“需要”或“不需要”)加入指示剂;
②计算得KMnO4溶液的c(KMnO4)=mol/L.(请写出最后化简结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一.煤转化为水煤气的主要化学反应为:C+H2O(g) ![]() CO+H2 . C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
CO+H2 . C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
①C(s)+O2(g)=CO2(g)△H1=﹣393.5kJmol﹣1;
②H2(g)+ ![]() O2(g)=H2O(g)△H2=﹣242.0kJmol﹣1;
O2(g)=H2O(g)△H2=﹣242.0kJmol﹣1;
③CO(g)+ ![]() O2(g)=CO2(g)△H3=﹣283.0kJmol﹣1;
O2(g)=CO2(g)△H3=﹣283.0kJmol﹣1;
试回答:
(1)请你根据以上数据,写出C(s)与水蒸气反应生成CO和H2的热化学方程式:
(2)比较反应热数据可知,1molCO(g)和1molH2(g)完全燃烧放出的热量之和,比1molC(s)完全燃烧放出的热量(填“多”或“少”).
甲同学据此认为:“煤炭燃烧时加少量水,可以使煤炭燃烧放出更多的热量”.乙同学根据盖斯定律作出了下列循环图
请你写出△H1、△H2、△H3、△H4之间存在的关系式 .
乙同学据此认为:“将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同.”请分析:甲、乙两同学的观点正确的是(填“甲”或“乙”)同学,另一同学出现错误观点的原因是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com