
【题目】用硫酸酸化的草酸(H2C2O4 , 二元弱酸)溶液能将KMnO4溶液中的MnO4﹣转化为Mn2+ . 某化学小组研究发现,少量MnSO4可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,请完成以下实验设计表.
实验 | 温度 | 初始pH | 0.1mol/L | 0.01mol/L | 蒸馏水 | 待测数据(反应混合液褪色 |
① | 常温 | 1 | 20 | 50 | 30 | t1 |
② | 常温 | 2 | 20 | 50 | 30 | t2 |
③ | 常温 | 2 | 40 | a | b | t3 |
表中a、b的值分别为:a=、b=
(2)该反应的离子方程式 .
(3)若t1<t2 , 则根据实验①和②得到的结论是
(4)请你设计实验④验证MnSO4对该反应起催化作用,完成表中内容.
实验方案(不要求写出具体操作过程) | 预期实验结果和结论 |
若反应混合液褪色时间小于实验①中的t1 , 则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
(5)某化学小组用滴定法测定KMnO4溶液物质的量浓度:取W g草酸晶体(H2C2O42H2O,其摩尔质量126g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定两次,平均消耗KMnO4溶液
V mL.请回答下列问题:
①该测定方法中(填“需要”或“不需要”)加入指示剂;
②计算得KMnO4溶液的c(KMnO4)=mol/L.(请写出最后化简结果)
【答案】
(1)50;10
(2)5H2C2O4+2MnO4﹣+6H+=10CO2↑+2Mn2++8H2O
(3)溶液的pH对该反应的速率有影响
(4)往反应混合液中加入少量MnSO4固体,控制其他反应条件与实验①相同,进行对比实验
(5)不需要;![]()
【解析】解:(1)实验要求控制KMnO4溶液初始浓度相同,则KMnO4溶液的体积为50mL,总体积为100mL,则水的体积10mL;
所以答案是:50;10;
(2.)草酸与高锰酸钾反应是锰离子和二氧化碳、水,其反应的离子方程式为:5H2C2O4+2MnO4﹣+6H+=10CO2↑+2Mn2++8H2O;
所以答案是:5H2C2O4+2MnO4﹣+6H+=10CO2↑+2Mn2++8H2O;
(3.)实验①和②只有pH不同,其它条件都相同,而且t1<t2 , 说明溶液的pH对该反应的速率有影响,
所以答案是:溶液的pH对该反应的速率有影响;
(4.)控制其他反应条件与实验①相同,加硫酸锰进行对比实验,若反应混合液褪色时间小于实验①中的t1 , 则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用);
所以答案是:
实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
往反应混合液中加入少量MnSO4固体,控制其他反应条件与实验①相同,进行对比实验 | 若反应混合液褪色时间小于实验①中的t1 , 则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
(5.)①高锰酸钾本身有颜色,故不需要另加指示剂,草酸反应完毕,加入最后一滴KMnO4溶液,溶液变为红色,红色30s内不褪去,说明滴定到终点,所以不需要加指示剂;
所以答案是:不需要;
②c(草酸)= ![]() =
= ![]() mol/L,
mol/L,
由关系式
2KMnO4 | ~ | 5H2C2O4 |
2 | 5 | |
cmolL﹣1×V×10﹣3L |
|
c= ![]() mol/L,
mol/L,
所以答案是: ![]() .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】准确称取6.0 g铝土矿样品(主要成分为Al2O3,含Fe2O3杂质),加入100 mL稀硫酸中,充分反应后向滤液中加入10 mol·L-1NaOH溶液,产生沉淀的质量和加入NaOH溶液体积之间的关系如图所示。则所用硫酸物质的量浓度为( )

A. 3.50 mol·L-1
B. 1.75 mol·L-1
C. 0.85 mol·L-1
D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列8种化学符号:168O2、188O2、H、126C、![]() Na、
Na、![]() 7N、146C、
7N、146C、![]() Mg。
Mg。
(1)表示核素的符号共________种。
(2)互为同位素的是______________。
(3)质量相同的H![]() O和D
O和D![]() O所含中子数之比为________。
O所含中子数之比为________。
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2 [Be(OH) 4]的离子方程式__________________。
(5)Be(OH) 2与Mg(OH)2可用_______________试剂鉴别。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质的方法错误的是( )
选项 | 物质 | 杂质 | 试剂 | 主要操作 |
A | SiO2 | Fe2O3 | 盐酸 | 过滤 |
B | Mg | Al | NaOH | 过滤 |
C | FeCl2 | FeCl3 | Cu | 过滤 |
D | KNO3 | KCl | H2O | 冷却结晶 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入 铜粉,最多能溶19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁 粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果不正确的是( )

A. 图中,AB段的反应为Fe+2Fe3+===3Fe2+,溶液中溶质最终为硫酸亚铁
B. 原溶液中硫酸浓度为2.5 mol·L-1
C. 原混合溶液中硝酸根离子的物质的量为0.4 mol
D. 图中,OA段产生的气体是一氧化氮,BC段产生的气体是氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 浓盐酸和浓硝酸均应保存在棕色试剂瓶中
B. 稀释浓硫酸时一定将水沿器壁缓缓注入浓硫酸中并不断搅拌
C. 滴瓶中的滴管用后不用清洗,直接放到滴瓶中
D. 温度计摔坏导致水银散落到地面上,应立即用水冲洗水银
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B是两种有刺激性气味气体。试根据下列实验事实填空。
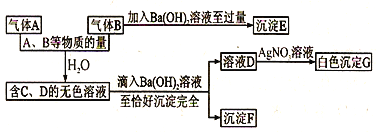
(1)写出C~F各物质的化学式: C______,D________,E_______,F_______。
(2)写出A、B跟水反应的离子方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法中正确的是( )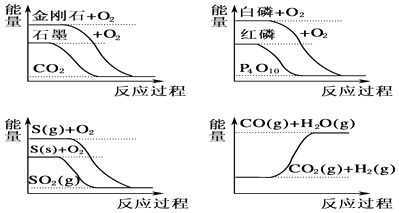
A.石墨转变为金刚石是吸热反应
B.白磷比红磷稳定
C.S(g)+O2(g)═SO2(g)△H1 , S(s)+O2(g)═SO2(g)△H2 , 则△H1>△H2
D.CO(g)+H2O(g)═CO2(g)+H2(g)△H>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com