
【题目】化合物Y具有抗菌、消炎作用,可由X制得:
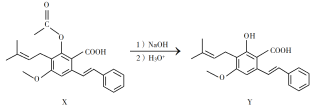
下列有关化合物X、Y的说法不正确的是
A.1 mol X最多能与3 mol NaOH反应
B.Y与乙酸乙酯在一定条件下反应可得到X
C.X、Y互为同系物
D.室温下X、Y分别与足量Br2加成的产物分子中手性碳原子数目相等
科目:高中化学 来源: 题型:
【题目】2020年3月9日,我国在西昌卫星发射中心用长征三号乙运载火箭,成功发射北斗系统第54颗导航卫星。长征三号乙运载火箭一二子级使用液体四氧化二氮和液体偏二甲肼(![]() ,又称1,1-二甲基联氨)作为推进剂,第三子级使用液氢和液氧作为推进剂,两组推进剂燃烧的产物均为无毒物质。下列说法正确的是( )
,又称1,1-二甲基联氨)作为推进剂,第三子级使用液氢和液氧作为推进剂,两组推进剂燃烧的产物均为无毒物质。下列说法正确的是( )
A.偏二甲肼分子中既有极性键也有非极性键,属于非极性分子
B.燃烧时每消耗![]() 偏二甲肼会转移
偏二甲肼会转移![]() 电子
电子
C.若![]() 液氢与足量液氧完全反应生成液态水会释放
液氢与足量液氧完全反应生成液态水会释放![]() 能量,则氢气的燃烧热为
能量,则氢气的燃烧热为![]()
D.两组推进剂燃烧的产物不会造成任何环境问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是
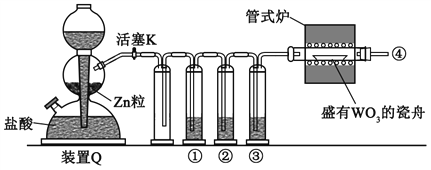
A. ①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
B. 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C. 结束反应时,先关闭活塞K,再停止加热
D. 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四苯基乙烯(TFE)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。以下是TFE的两条合成路线(部分试剂及反应条件省略):
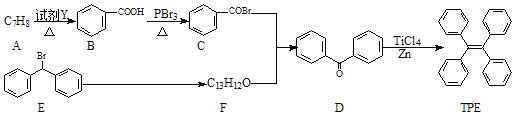
(1)A的名称是__;试剂Y为__。
(2)B→C的反应类型为__;B中官能团的名称是__,D中官能团的名称是__。
(3)E→F的化学方程式是___。
(4)W是D的同分异构体,具有下列结构特征:①属于萘(![]() )的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:__。
)的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:__。
(5)下列叙述正确的是__。
a.B的酸性比苯酚强
b.D不能发生还原反应
c.E含有3种不同化学环境的氢
d.TPE既属于芳香烃也属于烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向2 L密闭容器中充入2 mol N2和10 mol H2发生反应N2+3H2![]() 2NH3。2 min时测得剩余N2的物质的量为1 mol,下列有关化学反应速率的表达不正确的是
2NH3。2 min时测得剩余N2的物质的量为1 mol,下列有关化学反应速率的表达不正确的是
A. v(N2)=3 v(H2)B. v(H2)=0.75 mol·L-1·min-1
C. v(NH3)=0.5mol·L-1·min-1D. 再充入2 mol N2化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:298K时,N2(g)+3H2(g)![]() 2NH3(g) △H=-92.2kJ·mol-1。
2NH3(g) △H=-92.2kJ·mol-1。
(1)若N≡N的键能为941.3kJ·mol-1,H—H的键能为436.4kJ·mol-1,则N—H的键能为___。
(2)实验室将1.1molN2、3molH2充入2L容器,一定条件下反应。保持温度和容器体积不变,
①若2min末测得H2的物质的量为1.8mol,则该时间段内氨气的平均反应速率为___。
②保持温度和容器体积不变,下列措施可加快该反应速率的是___。
A.充入He气
B.使用恰当的催化剂
C.升高反应体系的温度
D.再充入N2
③当下列物理量保持不变时,表明该反应一定处于化学平衡状态的是___。
A.容器内N2与H2的含量
B.容器内气体密度
C.恒温下容器的压强
D.H2的物质的量
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示:
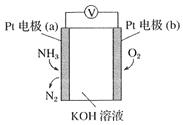
①外电路电流的运动方向:___。(填“a极到b极”或“b极到a极”)。
②b极电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用质量分数为36.5%的浓盐酸(密度为1.16 g·cm-3)配制成1 mol·L-1的稀盐酸。现实验室仅需要这种盐酸220 mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为________mL的容量瓶。
(2)在量取浓盐酸时宜选用下列量筒中的________。
A.5 mL B.10 mL C.25 mL D.50 mL
(3)在量取浓盐酸后,进行了下列操作:(将操作补充完整)
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,____________________________________________。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)________。
(4)若用1mol/L HCl溶液润洗容量瓶,再转移溶液,所配置的溶液浓度将_________(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以熔融的碳酸盐(K2CO3)为电解液,泡沫镍为电极,氧化纤维布为隔膜(仅允许阴离子通过)可构成直接碳燃料电池,其结构如图所示,下列说法正确的是
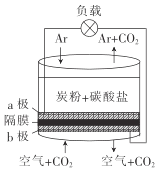
A.该电池工作时,CO32-通过隔膜移动到b极
B.若a极消耗1mol碳粉,转移电子数为4NA
C.b极的电极反应式为2CO2+O2-4e-=2CO32-
D.为使电池持续工作,理论上需要补充K2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com