
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,记录如下:
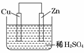 ①Zn为正极,Cu为负极。②H+向负极移动。③电子流动方向,从Zn经外电路流向Cu。④Cu极上有H2产生。⑤若有1 mol电子流过导线,则产生H2为0.5 mol⑥正极的电极反应式为:Zn-2e-===Zn2+描述合理的是( )
①Zn为正极,Cu为负极。②H+向负极移动。③电子流动方向,从Zn经外电路流向Cu。④Cu极上有H2产生。⑤若有1 mol电子流过导线,则产生H2为0.5 mol⑥正极的电极反应式为:Zn-2e-===Zn2+描述合理的是( )
A.①②③ B.③④⑤
C.④⑤⑥ D.②③④
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:

(1)“酸浸”中硫酸要适当过量,目的是 ▲ 。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42-,该反应的离子方程式为 ▲ 。
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定。有关反应的化学方程式如下:
2Fe3++Sn2++6Cl—=2Fe2++SnCl62—
Sn2++4Cl—+2HgCl2=SnCl62-+Hg2Cl2↓
6Fe2++Cr2O72—+14H+=6Fe3++2Cr3++7H2O
滴定时,K2Cr2O7标准溶液应盛放在 ▲ 滴定管中(填“酸式”、“碱式”);若不加HgCl2,则测定的Fe3+量 ▲ (填“偏高”、“偏低”或“不变”)。
(4)①可选用 ▲ (填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是 ▲ (用离子方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
实验可选用的试剂有:稀硝酸、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化: ▲ 。
b.沉淀: ▲ 。
c.分离,洗涤。
d.烘干,研磨。
查看答案和解析>>
科目:高中化学 来源: 题型:
非索非那定(化合物H)是一种重要的抗过敏药,其部分合成路线如下:
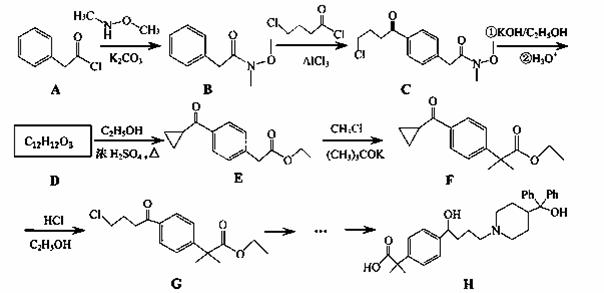
(1)B→C的反应类型为 ▲ ,E分子中含氧官能团有 ▲ (写名称)。
(2)D的结构简式为 ▲ 。
(3)F→G反应的化学方程式为 ▲ 。
(4)请写出一种同时满足下列条件的B的同分异构体的结构简式 ▲ 。
①苯环上有3个取代基;②具有α—氨基酸结构;③有6种不同化学环境的氢原子。
(5) 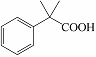 是一种重要的有机合成中间体,请完成以苯乙烯(
是一种重要的有机合成中间体,请完成以苯乙烯(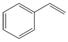 )为主要原料(其他试剂自选)合成该化合物的合成路线流程图。合成路线流程图示例如下:
)为主要原料(其他试剂自选)合成该化合物的合成路线流程图。合成路线流程图示例如下:
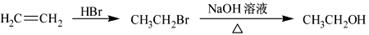
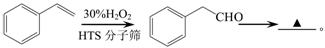
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于放热反应的是( )
A. 铁与盐酸反应 B. C与CO2共热
C. 碳酸钙的分解 D. Ba(OH)2·8H2O晶体与NH4Cl晶体反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将10mol A和5mol B放入10L真空箱内,某温度下发生反应:3A(g)+B(g) 2C(g)在最初0.2s内,消耗A的平均速率为0.06mol·(L·s)-1.则在0.2s时,真空箱中C的物质的量是( )
2C(g)在最初0.2s内,消耗A的平均速率为0.06mol·(L·s)-1.则在0.2s时,真空箱中C的物质的量是( )
A.0.12mol B.0.08mol C.0.04mol D.0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中元素________的非金属性最强;元素________的金属性最强 (填写元素符号);
(2)表中元素⑦的原子结构示意图是________;
(3)表中元素⑥⑩氢化物的稳定性顺序为________>________(填写化学式,下同);
(4)表中元素⑨和⑩最高价氧化物对应水化物的酸性:________>________;
(5) 表中元素最高价氧化物对应水化物的碱性最强的是:________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关X、Y、Z、W四种金属进行如下实验:
| 1 | 将X和Y用导线连接,浸入电解质溶液中,Y不易腐蚀 |
| 2 | 将片状的X、W分别投入等浓度盐酸中都有气体产生,W比X反应剧烈 |
| 3 | 用惰性电极电解等物质的量浓度的Y和Z的硝酸盐混合溶液,在阴极上首先析 |
根据以下事实,下列判断或推测错误的是( )
A.Z的阳离子氧化性最强 B.W的还原性强于Y的还原性
C.Z放入CuSO4溶液中一定有Cu析出 D.用X、Z和稀硫酸可构成原电池,且X做负极
查看答案和解析>>
科目:高中化学 来源: 题型:
将下列各组物质按酸、碱、盐分类顺次排列.正确的( )
|
| A. | 硝酸,乙醇,氯化钠 | B. | 硝酸,烧碱,纯碱 |
|
| C. | 硫酸,纯碱,胆矾 | D. | 盐酸,熟石灰,苛性钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com