
| A. | 升温 | B. | 改用粉末状大理石 | ||
| C. | 加入一定量水 | D. | 加入适量浓盐酸 |
科目:高中化学 来源: 题型:选择题
| A. | 燃料电池的电极包含活性物质,参与电极反应 | |
| B. | 氢氧燃料电池工作时发出蓝色火焰 | |
| C. | 铁在干燥的空气中不易生锈,在潮湿的空气中易生锈,主要是因发生电化腐蚀 | |
| D. | 温度一定时,催化剂不仅可以加快化学反应速率,而且可以改变反应物的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
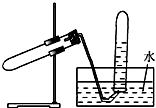 如图所示装置可用于( )
如图所示装置可用于( )| A. | 加热NaHCO3制CO2 | B. | 用Cu和浓HNO3反应制NO2 | ||
| C. | 用Zn与稀硫酸反应制H2 | D. | 用NaCl与浓H2SO4加热制HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
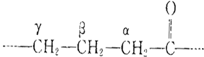

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
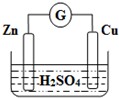
| A. | Zn是负极,Cu是正极 | B. | 稀硫酸溶液中H+移向Zn极 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 该装置能将电能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
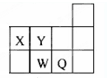
| A. | 元素X与元素Y可形成多种化合物 | |
| B. | 原子半径的大小顺序为:X>Y>W>Q | |
| C. | 还原性:W2-<Q- | |
| D. | 元素W的最高价氧化物对应水化物的酸性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 6 |
| V( 02 )/mL | 0.0 | 9.9 | 17.2 | 22.4 |
| A. | 0-2min的平均反应速率比4-6min快 | |
| B. | 0-6min 的平均反应速率v( H2O2)=3.3 x 10-2 moL-1•min-1 | |
| C. | 反应至 6min 时,c( H2O2)=0.3mol•L-1 | |
| D. | 反应至6min时,H2O2分解了 50% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A. | M的原子半径比Q的大 | |
| B. | L、T形成的简单离子核外电子数相等 | |
| C. | R、L、M三种元素的金属性依次增强 | |
| D. | Q、T两元素的氢化物的稳定性为H nT>H nQ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 化学键 | C═O | H-H | C-H | C-O | H-O |
| 键能/kJ•mol-1 | 803 | 436 | 414 | 326 | 464 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com