
【题目】对于乙苯有下列叙述:①所有的碳原子一定共平面;②能因与溴水反应而使溴水褪色;③可溶于CCl4中;④可溶于苯中;⑤能与浓硝酸发生取代反应。其中正确的是( )
A.①②③B.③④⑤C.②④⑤D.①③⑤
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】在无色透明溶液中,能大量共存的离子组是
A. Mg2+、Na+、SO42- B. K+、H+、HCO3-
C. Cu2+、NO3-、SO42- D. Ba2+、NO3-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋资源的利用具有广阔前景
(1)如图是从海水中提取镁的简单流程. 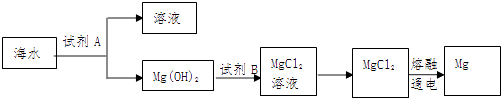
工业上常用于沉淀Mg2+的试剂A是 , Mg(OH)2转化为MgCl2的离子方程式是 .
(2)海带灰中富含以I﹣形式存在的碘元素,实验室提取I2的途径如下所示:
干海带 ![]() 海带灰
海带灰 ![]() 滤液
滤液 ![]()
![]()
![]() I2
I2
①灼烧海带至灰烬时所用的主要仪器名称是 .
②反应结束后,加入CCl4作萃取剂,采用萃取﹣分液的方法从碘水中提取碘,主要操作步骤如图: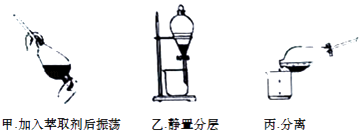
甲、乙、丙3步实验操作中,不正确的是(填“甲”、“乙”或“丙”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含0.2 mol KOH和0.1 mol Ba(OH)2的混合溶液中持续通入6.72 L(标况)CO2的过程中,溶液中离子的物质的量n和通入CO2体积V的关系示意图正确的是( )
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴的化合物用途广泛。一种利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等)制取CoCl2·6H2O粗品的工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式完全沉淀时的pH如下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2·6H2O熔点为86℃,加热至110℃~120℃时,失去结晶水生成无水氯化钴。
请回答下列问题:
(1)写出“浸出”时Co2O3发生反应的离子方程式:_______________________。
(2)加入NaClO3的作用是_________________________。
(3)萃取剂对金属离子的萃取率与pH的关系如下图所示。向“滤液Ⅱ”中加入萃取剂的主要目的是_______________,使用萃取剂时最适宜的pH__________(填字母序号)。
A.2.0~2.5 B.3.0~3.5 C.5.0~5.5 D.9.5~9.8

(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知某温度下,Ksp(MgF2)=7.35×10-11,Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)=__________。
(5)制得的CoCl2·6H2O粗品经进一步提纯得到CoCl2·6H2O晶体,在烘干晶体时需采用减压烘干,其原因是________________________。
(6)某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑等。充电时,该锂离子电池负极发生的反应为6C+xLi++xe-=LixC6。在电池充放电过程中,发生LiCoO2与Li1-xCoO2之间的转化,写出放电时电池反应方程式__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应的叙述正确的是
A.电解熔融MgCl2生成Mg(OH)2B.加热NH4Cl制备NH3
C.室温下,Al和Fe2O3反应生成FeD.铜和浓硝酸反应生成NO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com