
【题目】海洋资源的利用具有广阔前景
(1)如图是从海水中提取镁的简单流程. 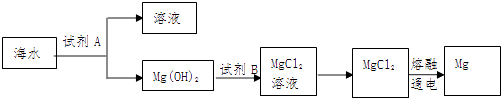
工业上常用于沉淀Mg2+的试剂A是 , Mg(OH)2转化为MgCl2的离子方程式是 .
(2)海带灰中富含以I﹣形式存在的碘元素,实验室提取I2的途径如下所示:
干海带 ![]() 海带灰
海带灰 ![]() 滤液
滤液 ![]()
![]()
![]() I2
I2
①灼烧海带至灰烬时所用的主要仪器名称是 .
②反应结束后,加入CCl4作萃取剂,采用萃取﹣分液的方法从碘水中提取碘,主要操作步骤如图: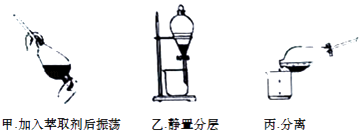
甲、乙、丙3步实验操作中,不正确的是(填“甲”、“乙”或“丙”).
【答案】
(1)石灰乳或氧化钙;Mg(OH)2+2H+=Mg2++2H2O
(2)坩埚;丙
【解析】解:(1)①工业上常用石灰乳或氧化钙沉淀Mg2+ , CaO和H2O反应生成Ca(OH)2 , Ca(OH)2和镁离子反应生成Mg(OH)2;氢氧化镁和盐酸反应得到氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O,所以离子方程式为Mg(OH)2+2H+=Mg2++2H2O,所以答案是:石灰乳或氧化钙;Mg(OH)2+2H+=Mg2++2H2O;(2)①灼烧固体时所用的主要仪器名称是坩埚,所以答案是:坩埚;②振荡、静置分层操持合理,而分离时先分离下层液体后倒出上层液体,则丙图不合理所以答案是:丙.


科目:高中化学 来源: 题型:
【题目】某Na2SO4不饱和溶液,加热蒸发掉30g水,未见晶体析出,与原溶液相比,没有发生变化的是( )
A.溶质的质量
B.溶质的质量分数
C.溶液的体积
D.溶液的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛性能优越,被称为继铁、铝之后的“第三金属”,工业上用钛矿石(主要成分:FeO、TiO2、SiO2等)为原料制取钛并得到副产物绿矾(FeSO4·7H2O),工艺流程如下,回答下列问题:

己知:①TiO2(s)+H2SO4(aq)=TiOSO4(aq)+H2O(l)
②TiO2+易水解,只能存在于强酸性溶液中
(1)钛矿石在加入浓硫酸酸溶前要先粉碎,其目的是_____________。
(2)加入过量铁粉的目的是_____________。
(3)固体2的主要成分是_____________。
(4)请用化学平衡移动原理解释溶液2加热煮沸的目的_____________。
(5)在高温下,TiO2和焦炭的混合物中通入Cl2得到TiC14和一种可燃性气体,请写出反应的化学方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e为元素周期表前3周期中的部分元素,它们在元素周期表中的相对位置如图所示.下列叙述正确的是( ) 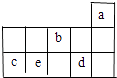
A.b元素除0价外,只有一种化合价
B.五种元素中,c元素的性质最稳定
C.d气态氢化物溶于水,溶液显碱性
D.e元素最高价氧化物对应的水化物和不同量的氢氧化钠反应,可能生成三种盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于乙苯有下列叙述:①所有的碳原子一定共平面;②能因与溴水反应而使溴水褪色;③可溶于CCl4中;④可溶于苯中;⑤能与浓硝酸发生取代反应。其中正确的是( )
A.①②③B.③④⑤C.②④⑤D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法正确的是( )
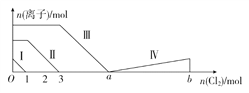
A. 线段Ⅱ表示Br-的变化情况 B. 线段Ⅳ表示IO3-的变化情况
C. 根据图象无法计算a的值 D. 原溶液中n(FeI2)∶n(FeBr2)=3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示,甲池的总反应式为:N2H4+O2=N2+2H2O,下列关于该电池工作时的说法正确的是
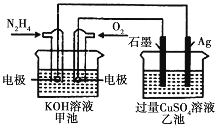
A. 该装置工作时,Ag电极上有气体生成
B. 甲池和乙池中的溶液的pH均减小
C. 甲池中负极反应为N2H4-4e-=N2+4H+
D. 当甲池中消耗0.1molN2H4时,乙池中理沦上最多产生6.4g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如下图所示,其中阴极和阳极均为惰性气体电极。测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是
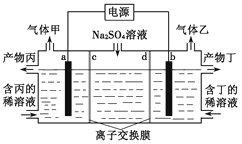
A. a极与电源的负极相连
B. 产物丁为硫酸溶液
C. 离子交换膜d为阴离子交换膜(允许阴离子通过)
D. b电极反立式为2H2O+2e-=2OH-+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com