
����Ŀ����2 L�ܱ������У�800��ʱ��Ӧ2NO(g)��O2(g)![]() 2NO2(g) ��H��0����ϵ�У�n(NO)��ʱ��ı仯���ұ���
2NO2(g) ��H��0����ϵ�У�n(NO)��ʱ��ı仯���ұ���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����( )
a��v(NO2)��2v(O2) b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2) d�����������ʵ��ܶȱ��ֲ���
��2����ͼ�б�ʾNO2�ı仯��������________��
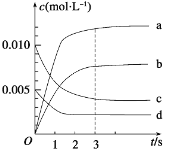
��3����O2��Ũ�ȱ仯��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��____________��
��4����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����( )
a�������������Ϊ1L b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч�Ĵ���
���𰸡���1��b c��2��b��3��0.0015 mol��L��1��s��1����4��a c��
��������
�����������1��a��δָ���������ʣ�������ʾͬһ����Ӧ���ʣ�v(NO2)��ʼ����Ϊv(O2)��2��������˵���ﵽƽ�⣬��a����b������������䣬�淴Ӧ���У���Ӧ��������ܵ����ʵ����ڼ�С��������ѹǿ��С����������ѹǿ���ֲ��䣬˵����Ӧ����ƽ�⣬��b��ȷ��c����ͬ���ʱ�ʾ���ʣ�����ƽ��ʱ����������֮�ȵ��ڻ�ѧ������֮�ȣ�V�� (NO)����(O2)=2��1����V�� (NO)=2v��(O2)����c��ȷ��d�������������������䣬�����ݻ�Ϊ��ֵ�������ܶ���ʼ���ղ��䣬����˵���ﵽƽ�⣬��d���ʴ�Ϊ��bc��
��2��NO2�������Ũ�ȴ�0��ʼ�����ݻ�ѧ����ʽ��NO��NO2�ļ�������ȣ���Ӧ��Ũ�ȵı仯��Ҳ��ȣ�����ƽ��ʱNO2��Ũ��С��0.01mol/L�����Ա�ʾNO2��Ũ�ȱ仯��������b�ߣ��ʴ�Ϊ��b��
��3������v=![]() ���NO�ķ�Ӧ����Ϊ
���NO�ķ�Ӧ����Ϊ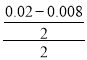 mol/(Ls)=0.003mol/(Ls)���ٸ�������֮�ȵ��ڼ�����֮�ȼ���O2��ƽ������Ϊ
mol/(Ls)=0.003mol/(Ls)���ٸ�������֮�ȵ��ڼ�����֮�ȼ���O2��ƽ������Ϊ![]() ��0.003mol/(Ls)=0.0015mol/(Ls)���ʴ�Ϊ��0.0015mol/(Ls)��
��0.003mol/(Ls)=0.0015mol/(Ls)���ʴ�Ϊ��0.0015mol/(Ls)��
��4��a�������������Ϊ1L���൱������ѹǿ��ƽ�������ƶ�����Ӧ���ʼӿ죬��ȷ��b���ʵ������¶ȣ��ӿ췴Ӧ���ʣ�����ӦΪ���ȷ�Ӧ��ƽ�������ƶ�������c������O2��Ũ�ȣ�ƽ�������ƶ���������Ũ�����ӣ����淴Ӧ���ʶ���ӿ죬��ȷ��d��ѡ���Ч�Ĵ���������ͬ�ȳ̶�������淴Ӧ���ʣ���ƽ�ⲻ�ƶ�������ѡac��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ�£�����������ĸ���Բ����ƿ�зֱ�������ٻ�������������HCl����NO2���������Ϊ4:1��NO2��O2��������Ȫʵ�顣����ַ�Ӧ����ƿ�����ʵ����ʵ���Ũ��֮��Ϊ
A��1:1:1 B��4: 4:5 C��5:5:4 D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪X��Y�ֱ���ԭ���������������A��B��C��D���ֶ�����Ԫ���е�������ɣ�A��B��Cͬ���ڣ���Cԭ�����γ�˫ԭ�������ӡ���֪������X�����ӻ���������Ӿ�����ͬ�ĵ��Ӳ�ṹ�����������Ȼ������Ҫ�ɷ֡�
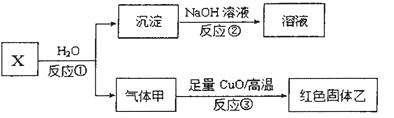
��1������ĵ���ʽ д����Ӧ���Ļ�ѧ����ʽ ��
��2������ɫ��������һ�ֵ��ʣ�д����Ӧ���Ļ�ѧ����ʽ ��
��3��������Ϊ�����л�����Cu2O�������ʵ��֤�� ��
����֪Cu2O+2H+==Cu+Cu2++H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ˮ�ۺ����õĹ�ҵ����ͼ���ж�����˵����ȷ���ǣ� ��
��֪��MgCl2��6H2O��������Mg(OH)Cl��HCl����ȡ�

A. ��ȥ���������ʣ�Mg2+��SO42����Ca2+���������ҩƷ˳��Ϊ��NaOH��Һ��Na2CO3��Һ��BaCl2��Һ�����˺������
B. �ڹ������н�MgCl2��6H2O���ռ����Ƶ���ˮMgCl2
C. ������ת���Ƕ��������ȼҵ�еĵ�ⱥ��ʳ��ˮ��һ������ѧ��ת��Ϊ���ܵĹ���
D. �ӵ���������������Ŀ����Ϊ���ᴿBr2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״���£���12gH2�������ȵ�N2
A. ����Ϊ12g B. ���ʵ���Ϊ6mol C. ���Ϊ22.4L D. ������Ϊ6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ʯ���ѽ�Ϊ��ϩ����ȡ����Ӧ
B. ��������к���̼��˫������������ʹ��ˮ��ɫ
C. ��������һ�������·���ˮ�ⷴӦ����������
D. C4H10����һ��ȡ�����������ַе㲻ͬ�IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǵ��CuCl2��Һ��װ�ã�����c��dΪʯī�缫���������йص��ж���ȷ���ǣ� ��
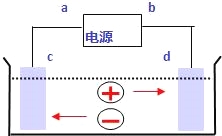
A��a������b����
B��a������b����
C���������У�d�缫��������
D���������У�������Ũ�Ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ʣ��ٱ����11.2LCO2 ��1g H2 ��1.204��1024��N2 ��4��ʱ18mLH2O������˵������ȷ���ǣ� ��
A�����Ӹ������ۣ��ܣ���=�� B��ԭ�Ӹ������ۣ��ܣ��٣���
C��������ۣ��ܣ���=�� D���������ۣ��٣��ܣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ��Na2O2��SO2![]() Na2SO4��Ƚϣ�Na2O2��������ͬ���ǣ���
Na2SO4��Ƚϣ�Na2O2��������ͬ���ǣ���
A. 2Na2O2��2CO2![]() Na2CO3+O2 B. 2Na2O2��2SO3
Na2CO3+O2 B. 2Na2O2��2SO3![]() 2Na2SO4+O2
2Na2SO4+O2
C. 2Na2O2+H2SO4![]() Na2SO4+H2O2 D. 3Na2O2+Cr2O3
Na2SO4+H2O2 D. 3Na2O2+Cr2O3![]() 2Na2CrO4+Na2O
2Na2CrO4+Na2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com