
【题目】同温同压下,三个等体积的干燥圆底烧瓶中分别充满:①混有少量空气的HCl;②NO2;③体积比为4:1的NO2和O2,进行喷泉实验。经充分反应后烧瓶内溶质的物质的量浓度之比为
A.1:1:1 B.4: 4:5 C.5:5:4 D.无法确定
【答案】C
【解析】
试题分析:同温同压下,等体积的气体的物质的量相等。①氯化氢极易溶于水,空气难溶于水,烧瓶内液体的体积是HCl的体积,设HCl的体积为V,则盐酸的物质的量浓度为V/Vm÷V=1/22.4mol/L;②二氧化氮和水反应方程式为:3NO2+H2O=2HNO3+NO,根据方程式知,水会充入烧瓶容积的2/3,溶液中的溶质是硝酸,其物质的量是二氧化氮的2/3,假设烧瓶的体积为1L,该条件下气体摩尔体积为Vm,则c(HNO3)2/3Vm÷2/3=1/22.4mol/L mol;③体积比为4:1的NO2和O2的混合气中,假设体积都为VL,根据以下方程式反应:4NO2+O2+2H2O=4HNO3,恰好反应无气体剩余,烧瓶内硝酸的体积为V,且生成硝酸物质的量为4V/(Vm×5)mol,所以溶质的物质的量浓度为1/Vm×5/4mol/L,所以所得三种溶液的物质的量浓度之比为![]() mol/L:
mol/L:![]() mol/L:(
mol/L:(![]() ×
×![]() )mol/L=5:5:4,答案选C。
)mol/L=5:5:4,答案选C。


科目:高中化学 来源: 题型:
【题目】甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物。实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验。
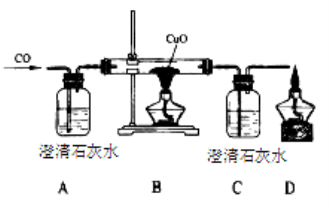
(1)B中反应的化学方程式是______________________,该反应的还原剂是________。
(2)实验过程中,C中的现象是____________,D处点燃酒精灯的目的是___________。
(3)对该实验的分析正确的是____________(选填编号)
A.实验结束时应先熄灭B处酒精灯
B.C中增加的质量与B中固体减小的质量相等
C.反应开始后通入0.1mol一氧化碳可生成0.1mol铜
D.反应结束后继续通入一氧化碳的目的是防止铜被氧化
(4)甲同学认识A装置用于证明一氧化碳不能和石灰水反应,乙同学认识省略A可达到同样的目的,理由是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【改编题】下列实验操作先后顺序正确的是( )
A.先装好药品,再检查装置的气密性
B.先用双手握紧试管,再将导管插入水中检查装置气密性
C.结束氢气还原氧化铜的实验时,先熄灭酒精灯后撤出导管
D.实验装置的组装顺序是从左到右,从上到下
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确是
A. 符合分子通式CnH2n+2的烃一定都是烷烃,分子中均只含单键
B. 通过石油裂化可以得到多种气态短链烃,其中包括重要化工原料
C. 苯能使溴水褪色,说明苯环结构中含有碳碳双键
D. 乙醇可以被氧气氧化成乙酸,但乙酸无法再被氧气氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:有机物A可发生如下图所示转化关系,且E能发生银镜反应,C不能发生银镜反应,则A的结构可能有(不考虑立体结构)

A.13种 B.9种 C.8种 D.10种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同.
(1)第四周期过渡元素的明显特征是形成多种多样的配合物
①CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5].羰基镍[Ni(CO)4].CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的离子为 (填化学式).
②金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测Ni(CO)4易溶于下列 .
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的.镓的基态原子的电子排布式是 ,Ga的第一电离能却明显低于Zn,原因是 .
(3)用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是 .
A.直线形;三角锥形
B.V形;三角锥形
C.直线形;平面三角形
D.V形;平面三角形.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器中,800℃时反应2NO(g)+O2(g)![]() 2NO2(g) △H<0,体系中,n(NO)随时间的变化如右表:
2NO2(g) △H<0,体系中,n(NO)随时间的变化如右表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)能说明该反应已经达到平衡状态的是( )
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
(2)右图中表示NO2的变化的曲线是________,
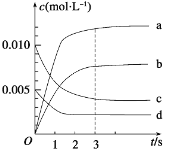
(3)用O2的浓度变化表示从0~2 s内该反应的平均速率v=____________。
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是( )
a.将容器体积变为1L b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com