
| A. | 氯气的分子式 Cl | B. | 钠原子的结构示意图 | ||
| C. | N2的电子式:N:::N: | D. | HClO的结构式 H-Cl-O |
分析 A.氯气为双原子分子,分子中含有两个氯原子;
B.钠原子的核电荷数=核外电子总数=11,最外层含有1个电子;
C.氮气分子中含有氮氮三键,氮氮三键的表示方法错误;
D.次氯酸的中心原子为O原子,分子中不存在H-Cl键.
解答 解:A.氯气分子中含有两个Cl原子,其正确的分子式为:Cl2,故A错误;
B.钠原子的核电荷数、核外电子总数都是11,其原子结构示意图为: ,故B正确;
,故B正确;
C.氮气分子中存在氮氮三键,氮原子最外层为8个电子,氮气正确的电子式为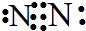 ,故C错误;
,故C错误;
D.次氯酸中含有1个氢氧键和1个O-Cl键,正确的结构式为:H-O-Cl,故D错误;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及分子式、原子结构示意图、电子式、结构式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的分析能力及规范答题能力.


 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:推断题
 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二. 无色,无气味并且易燃.是常见的一种基础能源.
无色,无气味并且易燃.是常见的一种基础能源. 有强氧化性的弱酸,可以用于消毒杀菌.
有强氧化性的弱酸,可以用于消毒杀菌.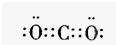 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L甲苯所含的分子数约为NA | |
| B. | 室温下,2.8g乙烯与丙烯的混合物中含碳原子的数目为0.2NA | |
| C. | 1 mol C30H62分子中含有共价键的数目为92NA | |
| D. | 1 mol氯气和足量甲烷在光照条件下反应可生成2NA个氯化氢分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 从结构的角度可以帮助我们更好的理解有机物的化学性质.
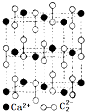
从结构的角度可以帮助我们更好的理解有机物的化学性质.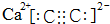 ,CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中有哑铃形C22-的存在,使晶胞沿一个方向拉长.CaC2晶体中1个Ca2+周围距离最近的C22-数目为4.已知CaC2晶体的密度为2.22g/cm3,该晶胞的体积为1.92×10-22cm3
,CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中有哑铃形C22-的存在,使晶胞沿一个方向拉长.CaC2晶体中1个Ca2+周围距离最近的C22-数目为4.已知CaC2晶体的密度为2.22g/cm3,该晶胞的体积为1.92×10-22cm3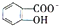 判断相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是
判断相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是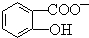 中-OH的氢原子形成分子内氢键,使其更难电离出H+.
中-OH的氢原子形成分子内氢键,使其更难电离出H+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数X>Y | B. | 离子半径X>Y | ||
| C. | X和Y一定在同一周期 | D. | X是第IIA族元素,Y是第VIIA族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
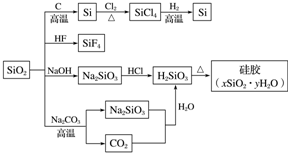
| A. | SiO2属于两性氧化物 | |
| B. | 盛放Na2CO3溶液的试剂瓶能用玻璃塞 | |
| C. | 图中所示转化反应都是氧化还原反应 | |
| D. | 硅胶吸水后可重复再生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | 除④⑥⑦以外 | C. | ③④⑤⑥ | D. | ②⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com