
【题目】溴单质具有广泛的工业价值,查阅资料知:Br2的沸点为59℃,微溶于水,有毒性.某化学小组模拟工业流程从浓缩的海水中提取液溴,主要实验装置(夹持装置略去)及操作步骤如下: 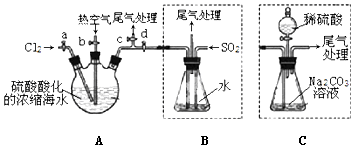
①连接A与B,关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③进行步骤②的同时,向B中通入足量SO2;
④关闭b,打开a,再通过A向B中缓慢通入足量Cl2;
⑤将B中所得液体进行蒸馏,收集液溴.
请回答:
(1)判断步骤①中反应已经结束的最简单方法为 .
(2)步骤②中鼓入热空气的作用为; 步骤③B中发生的主要反应的离子方程式为 .
(3)综合分析步骤①、②、③和④,这四步操作的最终目的为 .
(4)此实验中尾气可用(填选项字母)吸收处理. a.水 b.浓硫酸 c.NaOH溶液 d.饱和NaCl溶液
(5)步骤⑤中,蒸馏用到的玻璃仪器除酒精灯、温度计、尾接管、锥形瓶外,还有和;要达到提纯溴的目的,操作中应控制的关键条件为 .
(6)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸,再经步骤⑤,也能制得液溴.滴加稀硫酸之前,C中反应生成了NaBr、NaBrO3等,该反应的化学方程式为 .
【答案】
(1)A中液面上方出现黄绿色气体
(2)使A中生成的Br2随空气流进入B中;Br2+SO2+2H2O═4H++2Br﹣+SO42﹣
(3)富集溴
(4)c
(5)冷凝管(或冷凝器);蒸馏烧瓶;控制温度计温度,并收集59℃时的馏分
(6)3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑
【解析】解:(1)氯气为黄绿色气体,反应完毕应剩余氯气, 所以答案是:A中液面上方出现黄绿色气体;(2)溴易挥发,升高温度促进其挥发,所以通入热空气的目的是吹出Br2;二氧化硫具有还原性,把单质溴还原为溴离子,反应的方程式为Br2+SO2+2H2O═4H++2Br﹣+SO42﹣;
所以答案是:使A中生成的Br2随空气流进入B中;Br2+SO2+2H2O═4H++2Br﹣+SO42﹣;(3)步骤①制取溴,步骤②使溴挥发,步骤③吸收溴成溴离子,步骤④生成溴,故这四步操作的最终目的为富集溴,
所以答案是:富集溴;(4)氯气不可能完全反应,氯气和溴离子反应生成溴单质,未反应的二氧化硫、氯气和溴都有毒,不能直接排空,且这几种物质都能和碱反应,所以用碱液吸收;
所以答案是:c;(5)蒸馏需要蒸馏烧瓶、冷凝管、酒精灯、温度计、牛角管和锥形瓶等;达到提纯溴的目的,操作中应控制的关键条件是把温度控制在溴的沸点59°C,并收集该温度下的馏分,
所以答案是:冷凝管(或冷凝器);蒸馏烧瓶;控制温度计温度,并收集59℃时的馏分;(6)根据题给信息,溴和碳酸钠反应生成了溴化钠和溴酸钠,据此写出反应方程式为:Br2+Na2CO3→NaBr+NaBrO3 , 根据化合价升降总数相等配平为:3Br2+3Na2CO3→5NaBr+NaBrO3 , 根据原子守恒,还有产物二氧化碳3mol,故反应方程式为:3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑,
所以答案是:3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】除去下列物质中所含杂质(括号中的物质)所选用的试剂和装置均正确的是( )
Ⅰ.试剂:
①KMnO4/H+②NaOH溶液③饱和Na2CO3溶液④H2O⑤Na⑥Br2/H2O⑦Br2/CCl4
Ⅱ.装置:
选项 | 物质 | 试剂 | 装置 |
A | C2H6(C2H4) | ⑥ | ① |
B | 苯(苯酚) | ① | ③ |
C | CH3COOC2H5(CH3COOH) | ③ | ② |
D | 甲苯(二甲苯) | ⑦ | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:
①MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O
②Cl2+SO2+2H2O=H2SO4+2HCl
(1)反应①的离子方程式;
(2)反应①中被氧化的HCl和未被氧化的HCl的物质的量之比为 , 有0.2mol HCl被氧化,转移电子的数目是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生以铁丝和Cl2为原料进行下列三个实验.从分类角度分析,下列选项正确的是( ) 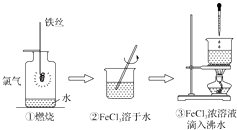
A.实验①、②所涉及的物质均为电解质
B.实验②、③均为放热反应实验
C.②、③均未发生氧化还原反应
D.实验①、③反应制得的物质均为纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,①6.72L NH3②1.204×1023个 H2S ③6.4g CH4④0.5mol HCl,下列关系正确的是( )
A.体积大小:④>③>②>①
B.密度大小:④>②>③>①
C.原子数目:③>①>④>②
D.质量大小:④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的化工原料,我们已学过用两种方法制得乙烯: 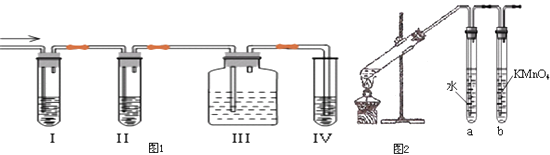
A.在实验室里用乙醇与浓硫酸共热制乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计如图1以确认上述混合气体中有C2H4和SO2 . 回答下列问题:
(1)I、II、III、IV装置中,可盛放的试剂顺序是(将下列有关试剂的序号填入空格内).
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是 .
(3)确定含有乙烯的现象是 .
(4)写出生成乙烯的反应方程式: .
B.为检验利用溴乙烷发生消去反应后生成的气体中是否含乙烯的装置如图2所示.回答:
①利用溴乙烷发生消去反应的化学方程式为:;
②试管a的作用是;若省去试管a,试管b中试剂为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国政府规定在2006年7月1日后含有铜、铬、镉、汞、多溴联苯等材料的电子产品禁止投放市场。下列有关电子垃圾的说法中不正确的是( )
A.电子垃圾应在无污染的条件下回收,使之成为有用的资源
B.将电子垃圾在火上焚烧,熔下其中的金属再回收利用
C.电子垃圾的任意抛弃会严重污染地下水源
D.各国的电子垃圾应在本国境内处理,严禁向其他国家输出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com