
| A.NaCN | B.NaF | C.CH3COONa | D.NaNO2 |
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.比较等体积、等pH值的两种溶液的导电性 |
| B.比较等物质的量浓度的氯化钠与醋酸钠溶液的pH值 |
| C.比较等体积、等pH值的两种溶液与过量锌粉反应产生氢气的量 |
| D.比较等体积、等物质的量浓度的两种溶液稀释相同倍数后的pH变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A. | B. |
C. | D.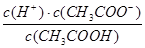 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液的pH增大 | B.CH3COOH的电离程度增大 |
| C.溶液的导电能力减小 | D.溶液的c(OH-)减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 NH4++ NH2- , 据此判断以下叙述错误的是
NH4++ NH2- , 据此判断以下叙述错误的是 | A.液氨中含有NH3、NH4+、NH2-等粒子 |
| B.一定温度下,液氨中c (NH4+) · c (NH2-) 是一个常数 |
| C.液氨的电离达到平衡时,c (NH3) = c(NH4+) = c (NH2-) |
| D.只要不加入其他物质,液氨中c (NH4+) = c (NH2-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.强电解质的导电能力一定大于弱电解质的导电能力 |
| B.溶于水能导电的化合物都是电解质 |
| C.25℃时,0.1mol/L的盐酸中氢离子浓度大于0.1mol/L的醋酸中氢离子浓度 |
| D.BaSO4属于强电解质,所以其水溶液导电能力很强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(OH-)/c(NH3·H2O) | B.c(NH3·H2O)/c(OH-) |
| C.n(OH-) | D.c(H﹢) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
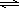 H++In—(aq)
H++In—(aq)| A.(1)(4)(5) | B.(2)(5)(6) |
| C.(1)(4) | D.(2)(3)(6) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com