
【题目】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的电子式____________,结构简式____________。
(2)鉴别甲烷和乙烯的试剂是______(填序号)。
a.稀硫酸 b.溴的四氯化碳溶液 c.水 d.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是______(填序号)。
a.CH3CH3 b.CH3CHCl2 c.CH3CH2OH d.CH3CH2Br
(4)已知 2CH3CHO+O2![]() 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示:
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示:
![]()
反应②的化学方程式为_________。 工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为_____________,反应类型是__________。
【答案】![]() CH2=CH2 bd acd 2CH3CH2OH+O2
CH2=CH2 bd acd 2CH3CH2OH+O2![]() 2CH3CHO+2H2O nCH2 =CH2
2CH3CHO+2H2O nCH2 =CH2 ![]()
![]() 加聚反应
加聚反应
【解析】
(1)略
(2)甲烷化学性质比较稳定,和强酸、强碱、强氧化剂之间均不发生反应,在一定条件下能与氯气,氧气反应,在高温下可以发生分解反应,生成碳和氢气;乙烯能与溴的四氯化碳溶液发生加成反应,而使溶液褪色,能与高锰酸钾溶液发生氧化还原反应而使溶液褪色;
(3)乙烯和水加成能生成乙醇,和氢气加成生成乙烷,和溴化氢加成生成溴乙烷;
(4)乙烯和水发生加成反应,生成乙醇,乙醇氧化生成乙醛,乙醛再氧化,最终生成乙酸,因而A为CH3CH2OH,B为CH3CHO。
(1)乙烯的结构简式为CH2=CH2,电子式为:![]() ;
;
(2)乙烯能与溴的四氯化碳溶液发生加成反应,而使溶液褪色,能与高锰酸钾溶液发生氧化还原反应而使溶液褪色,甲烷与溴的四氯化碳溶液和高锰酸钾溶液均不反应,可用溴的四氯化碳溶液和高锰酸钾溶液检验两种物质;
(3)乙烯和水加成能生成乙醇,和氢气加成生成乙烷,和溴化氢加成生成溴乙烷,答案选acd;
(4)乙烯和水发生加成反应,生成乙醇,乙醇氧化生成乙醛,乙醛再氧化,最终生成乙酸,因而A为CH3CH2OH,B为CH3CHO,反应②为乙醇催化氧化的反应,方程式为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;以乙烯为原料可以生产一种重要的合成有机高分子化合物为聚乙烯,反应方程式为:nCH2 =CH2
2CH3CHO+2H2O;以乙烯为原料可以生产一种重要的合成有机高分子化合物为聚乙烯,反应方程式为:nCH2 =CH2 ![]()
![]() ,反应属于加聚反应。
,反应属于加聚反应。


科目:高中化学 来源: 题型:
【题目】.在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明反应: A(s)+3B(g)![]() 2C(g)+D(g)已达平衡状态的是
2C(g)+D(g)已达平衡状态的是
A. 混合气体的压强B. 混合气体的密度
C. 3v逆(C)=2v正(B)D. 气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世界某著名学术刊物介绍了一种新型中温全瓷铁空气电池,其结构如图所示。

下列有关该电池放电时的说法正确的是( )
A.a极发生氧化反应
B.正极的电极反应式为FeOx+2xe-=Fe+xO2-
C.若有22.4 L(标准状况)空气参与反应,则电路中有4 mol电子转移
D.铁表面发生的反应为xH2O(g)+Fe=FeOx+xH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是( )
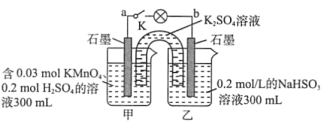
A.电池工作时,甲烧杯发生的反应为MnO4-被还原生成MnO2
B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a
C.乙中电极反应为HSO3--2e-+H2O=SO42-+3H+
D.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的H+浓度约为0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。利用“KClO3氧化法”制备KIO3工艺流程如图所示:

已知:酸化反应产物有KH(IO3)2、Cl2和KCl
(1)“酸化反应”所需I2从海带中提取。经历灼烧海带,浸泡海带灰等步骤,向获得的I-溶液加入MnO2,在酸性条件下生成I2,其离子反应方程式为___。
(2)酸化产物KH(IO3)2所含化学键有___,“调pH”中发生反应的化学方程式为___。
(3)已知KIO3在水中随温度升高而增大,则浓缩结晶的具体步骤是___。
(4)KIO3也可采用“电解法”制备,装置如图所示。

①KOH与I2制备KIO3的离子反应方程式为___。
②电解时阳极的电极反应式:___;阴极的电极反应式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z、W四种元素的符号: X________、Y__________、Z____________、W、________
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为__________________,______________________。
(3)由X、Y、Z所形成的离子化合物是________________,它与W的最高氧化物的水化物的浓溶液加热时反应的离子方程式是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,将NO(g)和O2(g)按物质的量之比2∶1充入反应容器,发生反应:2NO(g) + O2(g) ![]() 2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如下图所示。下列说法正确的是
2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如下图所示。下列说法正确的是

A. p1 < p2
B. 其他条件不变,温度升高,该反应的反应限度增大
C. 400℃、p1条件下,O2的平衡转化率为20%
D. 400℃时,该反应的化学平衡常数的数值为10/9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不能正确表示下列变化的离子方程式是
A.BaCO3溶于盐酸:BaCO3+2H+=Ba2++CO2↑+H2O
B.FeCl3溶液腐蚀铜板:2Fe3++Cu=2Fe2++Cu2+
C.苯酚钠溶液中通入少量CO2:2![]() +CO2+H2O=2
+CO2+H2O=2![]() +CO32—
+CO32—
D.醋酸钠水解:CH3COO+H2O![]() CH3COOH+OH
CH3COOH+OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将1 mol气体A和1 mol气体B充入2 L某密闭容器中,发生反应:![]() ,
,![]() 时达到平衡。在
时达到平衡。在![]() 、
、![]() 时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化的曲线如图所示。下列说法正确的是( )
时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化的曲线如图所示。下列说法正确的是( )
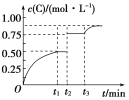
A.![]() 时改变的条件是使用催化剂
时改变的条件是使用催化剂
B.反应的化学方程式中,![]()
C.![]() 间该反应的平衡常数均为5
间该反应的平衡常数均为5
D.![]() 时改变的条件是移去少量物质D
时改变的条件是移去少量物质D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com