
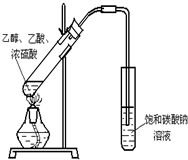
 某实验小组用如图装置制取乙酸乙酯,请回答下列问题:
某实验小组用如图装置制取乙酸乙酯,请回答下列问题:| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
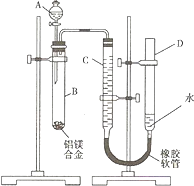 (2008?重庆)某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.
(2008?重庆)某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.| 33600(a-c) |
| b |
| 33600(a-c) |
| b |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 物质 | 沸点 |
| 乙醚 | 34.6℃ |
| 乙醇 | 78.2℃ |

| △ |
| △ |
| 浓硫酸 |
| 170℃ |
| △ |
| △ |
| △ |
| 浓硫酸 |
| 170℃ |
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:
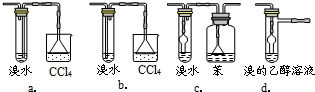
 电化学法可消除甲醇(CH3OH)对水质造成的污染.其原理是:通电后Co2+被氧化成Co3+,生成的Co3+把水中的甲醇氧化:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+.某学习小组用如图装置进行实验.下列说法错误的是( )
电化学法可消除甲醇(CH3OH)对水质造成的污染.其原理是:通电后Co2+被氧化成Co3+,生成的Co3+把水中的甲醇氧化:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+.某学习小组用如图装置进行实验.下列说法错误的是( )查看答案和解析>>
科目:高中化学 来源:2012年上海市浦东新区高考化学二模试卷(解析版) 题型:填空题
| 物质 | 沸点 |
| 乙醚 | 34.6℃ |
| 乙醇 | 78.2℃ |



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com