
【题目】有机物F是有机合成工业中一种重要的中间体.以甲苯和丙烯为起始原料合成F的工艺流程如图: 
回答下列问题:
(1)化合物B中含氧官能团名称是F的结构简式
(2)写出C与银氨溶液共热的化学反应方程式:
(3)化合物D不能发生的反应有(填序号). ①加成反应 ②取代反应 ③消去反应 ④氧化反应 ⑤水解反应
(4)B的含苯环结构的同分异构体还有种,其中一种的核磁共振氢谱中出现4个峰且不与FeCl3溶液发生显色反应的是(填结构简式).
(5)B与D发生反应的类型 .
【答案】
(1)酚羟基;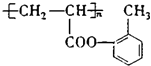
(2)CH2=CHCHO+2Ag(NH3)2OH ![]() CH2=CHCOONH4+2Ag↓+3NH3+H2O
CH2=CHCOONH4+2Ag↓+3NH3+H2O
(3)③⑤
(4)4;![]()
(5)取代反应
【解析】解:(1)由以上分析可知化合物B为 ![]() ,含氧官能团名称是酚羟基,F的结构简式为
,含氧官能团名称是酚羟基,F的结构简式为 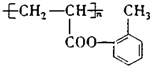 , 所以答案是:酚羟基;
, 所以答案是:酚羟基; 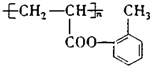 ;(2)C与银氨溶液共热的化学反应方程式:CH2=CHCHO+2Ag(NH3)2OH
;(2)C与银氨溶液共热的化学反应方程式:CH2=CHCHO+2Ag(NH3)2OH ![]() CH2=CHCOONH4+2Ag↓+3NH3+H2O,
CH2=CHCOONH4+2Ag↓+3NH3+H2O,
所以答案是:CH2=CHCHO+2Ag(NH3)2OH ![]() CH2=CHCOONH4+2Ag↓+3NH3+H2O;(3)化合物D为CH2=CHCOOH,含有碳碳双键,可以发生加成反应、氧化反应,能燃烧,属于氧化反应,含有羧基,可以发生取代反应,不能发生消去反应与水解反应,
CH2=CHCOONH4+2Ag↓+3NH3+H2O;(3)化合物D为CH2=CHCOOH,含有碳碳双键,可以发生加成反应、氧化反应,能燃烧,属于氧化反应,含有羧基,可以发生取代反应,不能发生消去反应与水解反应,
所以答案是:③⑤;(4)B为 ![]() ,其同分异构体含苯结构,羟基、甲基还有间位、对位两种,侧链可以为﹣OCH3或﹣CH2OH,符合条件的同分异构体共有4种,其中核磁共振氢铺有4组峰,且不与氯化铁显色的结构为
,其同分异构体含苯结构,羟基、甲基还有间位、对位两种,侧链可以为﹣OCH3或﹣CH2OH,符合条件的同分异构体共有4种,其中核磁共振氢铺有4组峰,且不与氯化铁显色的结构为 ![]() ,
,
所以答案是:4; ![]() ;(5)B为
;(5)B为 ![]() ,D为CH2=CHCOOH,二者发生取代反应生成
,D为CH2=CHCOOH,二者发生取代反应生成 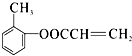 ,
,
所以答案是:取代反应.


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】(15分)水中溶解氧是水生生物生存不可缺少的条件.某课外小组采用碘量法测定学校周边河水中的溶解氧.实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样.记录大气压及水体温度.将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2 , 实现氧的固定.
Ⅱ.酸化,滴定
将固氧后的水样酸化,MnO(OH)2被I﹣还原为Mn2+ , 在暗处静置5min,然后用标准Na2S2O3溶液滴定生成的I2(2S2O32﹣+I2=2I﹣+S4O62﹣).
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是 .
(2)“氧的固定”中发生反应的化学方程式为 .
(3)Na2S2O3溶液不稳定,使用前需标定.配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶和;蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除及二氧化碳.
(4)取100.00mL水样经固氧、酸化后,用a molL﹣1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为;若消耗Na2S2O3溶液的体积为b mL,则水样中溶解氧的含量为mgL﹣1 .
(5)上述滴定完成后,若滴定管尖嘴处留有气泡会导致测量结果偏 . (填“高”或“低”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳跟浓硫酸共热产生的混合气体X和铜跟浓硝酸反应产生的混合气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )

A. 洗气瓶中产生的沉淀是BaCO3
B. 在Z导管出来的气体中无CO2
C. 洗气瓶中产生的沉淀是BaSO3
D. 在Z导管口有红棕色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示示意图,下列说法不正确的是( )

A. 反应C(s)+H2O(g)![]() CO(g)+H2(g) 能量增加(b-a) kJ·mol-1
CO(g)+H2(g) 能量增加(b-a) kJ·mol-1
B. 该反应过程反应物断键吸收的能量大于生成物成键放出的能量
C. 1mol C(s)和1mol H2O(l)反应生成1mol CO(g)和1mol H2(g)吸收热量131.3 kJ
D. 1 mol C(g)、2 mol H、1 mol O转变成1 mol CO(g)和1 mol H2(g)放出的热量为a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铁具有独有的脱色能力,适用于染料、染料中间体、印染、造纸行业的污水处理.某课题小组设计如下方案制备氯化亚铁并探究氯化亚铁(Fe2+)的还原性.某同学选择下列装置用氯化铁制备少量氯化亚铁(装置不可以重复使用).查阅资料知,氯化铁遇水剧烈水解,在加热条件下氢气还原氯化铁生成FeCl2 . 
(1)实验开始前应先检查装置的气密性,请叙述装置A气密性检验的方法:
(2)气流从左至右,装置接口连接顺序是a
(3)装置C中干燥管中所盛试剂的名称是: , 作用是:
(4)装置D中发生的化学方程式是:
(5)为了测定氯化亚铁的质量分数,某同学进行了如下实验: 称取实验制备的氯化亚铁样品5.435g,配成溶液,用1.00molL﹣1酸性KMnO4标准溶液滴定至终点.(已知还原性Fe2+>Cl﹣)滴定结果如表所示:
滴定次数 | 标准溶液的体积 | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 1.04 | 25.03 |
2 | 1.98 | 25.99 |
3 | 3.20 | 25.24 |
①写出滴定过程中所发生的2个离子方程式 ,
②样品中氯化亚铁的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原子结构及元素周期律的知识,下列推断正确的是( )
A.![]() Cl2与
Cl2与 ![]() Cl2氧化能力相近,二者互为同位素
Cl2氧化能力相近,二者互为同位素
B.![]() Se与
Se与 ![]() Se所含质子数相同,中子数不同
Se所含质子数相同,中子数不同
C.同主族元素形成的含氧酸的酸性随核电荷数的增加而减弱
D.同周期主族元素形成的简单离子半径随核电荷数的增大而减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种工业制备SrCl6H2O的生产 流程如下:
已知:①M(SrCl26H2O)=267g/mol;
②Ksp(SrSO4)=3.3×10﹣7、Ksp(BaSO4)=1.1×10﹣10;
③经盐酸浸取后,溶液中除含有Sr2+和Cl﹣外,还含有少量Ba2+杂质.
(1)隔绝空气高温焙烧,若2mol SrSO4中只有S被还原,转移了16mol电子.写出该反应的化学方程式: .
(2)过滤2后还需进行的两步操作是、 .
(3)加入硫酸的目的是;为了提高原料的利用率,滤液中Sr2+的浓度应不高于 mol/L(注:此时滤液中Ba2+浓度为1×10﹣5 mol/L).
(4)产品纯度检测:称取1.000g产品溶解于适量水中,向其中加入含AgNO31.100×10﹣2 mol的AgNO3溶液(溶液中除Cl﹣外,不含其它与Ag+反应的离子),待Cl﹣完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000mol/L的NH4SCN标准溶液滴定剩余的AgNO3 , 使剩余的Ag+ 以AgSCN白色沉淀的形式析出.
①滴定反应达到终点的现象是 .
②若滴定过程用去上述浓度的NH4SCN溶液20.00mL,则产品中SrCl26H2O的质量百分含量为(保留4位有效数字).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com