
| A.HCl最快; | B.H2SO4最快; | C.CH3COOH最快; | D.一样快 |
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数(mol2·L-2) | 1×10-14 | a | 1×10-12 |
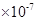 4.0
4.0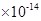 ②
② ①
① ③
③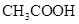
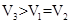 D (3)
D (3)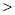
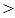
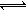 HCO3- + OH- (1分)
HCO3- + OH- (1分)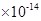 。酸性越弱,相应的钠盐越容易水解,溶液的碱性就越强。酸性是醋酸>碳酸>次氯酸。所以如果测得① Na2CO3(aq)② CH3COONa(aq)③ NaClO(aq)三种稀溶液的pH值相同。那么,它们的物质的量浓度由大到小的顺序是②
。酸性越弱,相应的钠盐越容易水解,溶液的碱性就越强。酸性是醋酸>碳酸>次氯酸。所以如果测得① Na2CO3(aq)② CH3COONa(aq)③ NaClO(aq)三种稀溶液的pH值相同。那么,它们的物质的量浓度由大到小的顺序是② ①
① ③。
③。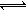 HCO3- + OH-。
HCO3- + OH-。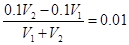 ,解得V1∶V2=9:11。溶液中各种离子的浓度由大到小的顺序是c (Na+) >c(SO42-)>c (H+) >c (OH-)。
,解得V1∶V2=9:11。溶液中各种离子的浓度由大到小的顺序是c (Na+) >c(SO42-)>c (H+) >c (OH-)。

 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:不详 题型:单选题
| A.能使石蕊试液呈蓝色的溶液:Na+、I-、Cl-、NO3- |
| B.含大量Fe3+的溶液:NH4+、Na+、Cl-、SCN- |
| C.能与Al反应生成H2的溶液:Ca2+、NH4+、HCO3-、Cl- |
| D.水电离出的c(H+)=1×10-14mol/L的溶液:K+、AlO2-、Br-、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H2SO3 + OH- ①
H2SO3 + OH- ① H+ + SO32- ②
H+ + SO32- ②| A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 |
B.加入少量Na2SO3固体,则c(H+) + c(Na+) = c(HSO3-) + c(OH-) +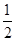 c(SO32-) c(SO32-) |
C.加入少量NaOH溶液,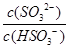 、 、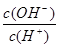 的值均增大 的值均增大 |
| D.加入氨水至中性,则2c(Na+) = c(SO32-)>c(H+) = c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.Na+、H+、Cl-、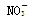 | B.K+、Ba2+、OH-、I- |
| C.Cu2+、Na+、Br-、Cl- | D.Na+、K+、Cl-、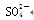 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Al3+、K+、NO3- | B.Fe2+、Na+、NO3- |
| C.Na+、Cl一、HCO3- | D.Na+、SO32一、S2- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NO3-、Cl-、Na+、H+ | B.AlO2-、K+、ClO- CO32- |
| C.Ca2+、Cl-、SO42-、Na+ | D.SO42-、Fe2+、OH-、NH4+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、Fe2+、SO42-、Cl― |
| B.Ag+、Al3+、H+、NO3― |
| C.Na+、K+、SO42-、SO32- |
| D.NH4+、Ca2+、NO3―、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H+、K+、Fe2+、NO | B.OH-、Cl-、Na+、NH4+ |
| C.Mg2+、K+、Cl-、NO | D.I-、Cl-、H+、Fe3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Mg2+、Fe3+、NO3-、SCN- | B.Al3+、Fe2+、Cl-、SO42- |
| C.K+、Na+、Cl-、HCO3- | D.Na+、Ba2+、NO3-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com