
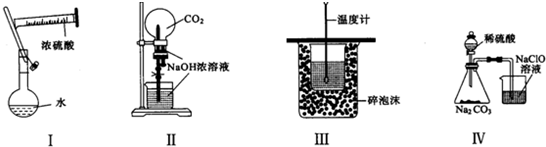
| A. | 实验Ⅰ:配制一定物质的量浓度的稀硫酸 | |
| B. | 实验Ⅱ:用二氧化碳作喷泉实验 | |
| C. | 实验Ⅲ:进行中和热的测定 | |
| D. | 实验Ⅳ:验证酸性的强弱,H2SO4>H2CO3>HClO |
分析 A.容量瓶只能配制一定物质的量浓度溶液,不能溶解或稀释药品;
B.该气体极易溶于该溶液形成大的压强差时就能做喷泉实验;
C.必须有环形玻璃搅拌棒搅拌混合溶液;
D.二氧化碳和次氯酸反应没有明显现象.
解答 解:A.一定浓度溶液的配制,应该先在烧杯中稀释冷却后在转移到容量瓶内,故A错误;
B.打开弹簧夹,挤压胶头滴管,能形成大的压强差,可以产生喷泉,故B正确;
C.缺少环形玻璃搅拌棒,否则导致混合溶液温度不均匀,故C错误;
D.二氧化碳通入NaClO溶液中会生成HClO,但是该反应没有现象,无法通过该实验看出是否有HClO生成,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及实验基本操作、物质检验等知识点,明确实验原理及物质性质、实验基本操作方法、实验仪器的用途等知识点是解本题关键,易错选项是C,注意不能用金属作搅拌棒,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素最高化合价的顺序为Z>Y>T>X | |
| B. | Y、Z分别形成的简单氢化物的稳定性为Z>Y | |
| C. | 由X、Y和Z三种元素构成的强电解质,对水的电离均起抑制作用 | |
| D. | 常温下,T的单质与Y的最高价氧化物对应水化物的浓溶液不能反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 沸点 | 溶解性 | 着火点(闪点) | 毒性 | |
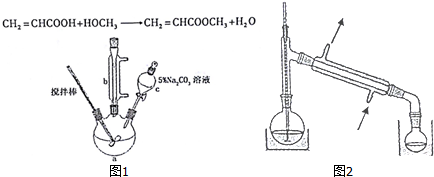
| 丙烯酸 | 142℃ | 与水互溶,易溶于有机溶剂 | 54℃ | 有毒 |
| 甲醇 | 65℃ | 与水互溶,易溶于有机溶剂 | 11℃ | 有毒 |
| 丙烯酸甲酯 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 不详 | 无毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
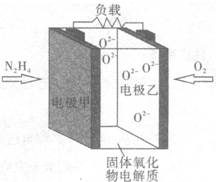 液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.某科研人员设计了以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池(如图所示).该固体氧化物电解质的工作温度高达700~900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质.下列说法正确的是( )
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.某科研人员设计了以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池(如图所示).该固体氧化物电解质的工作温度高达700~900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质.下列说法正确的是( )| A. | 电极甲为电池正极 | |
| B. | 电池总反应为N2H4+2O2═2NO+2H2O | |
| C. | 电池正极反应式为O2+2H2O+4e-═4OH- | |
| D. | 图示中的O2-由电极乙移向电极甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数大小顺序为Z>Y>X | B. | W、X的简单离子能抑制水的电离 | ||
| C. | 单质的熔点大小顺序为X>W>Y | D. | 原子半径大小顺序为X>Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径Z>X>Y | |
| B. | 最高价氧化物的水化物酸性强弱W>Z>Y | |
| C. | 简单气态氢化物的稳定性Z>W | |
| D. | W分别与X、Y形成的化合物化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com