
| A. | Al元素的第一电离能比Mg元素的大 | |
| B. | 第2周期元素的最高正化合价都等于其原子的最外层电子数 | |
| C. | 同一周期主族元素从左到右,原子半径和离子半径均逐渐减小 | |
| D. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
分析 A.Mg元素原子3s能级容纳2个电子,为全满稳定状态,能量较低,第一电离能高于同周期相邻元素;
B.氧元素、氟元素没有最高正化合价;
C.同一周期主族元素从左到右,原子半径减小,电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多,离子半径越大;
D.非金属性越强,最高价含氧酸的酸性越强.
解答 解:A.Mg元素原子3s能级容纳2个电子,为全满稳定状态,能量较低,第一电离能高于同周期相邻元素,故Al元素的第一电离能比Mg元素的小,故A错误;
B.氧元素、氟元素没有最高正化合价,故B错误;
C.同一周期主族元素从左到右,原子半径减小,阳离子半径减小,阴离子半径也减小,且阳离子半径小于阴离子半径,故C错误;
D.非金属性酸Cl>S>P>Si,非金属性越强,最高价含氧酸的酸性越强,故酸性:HClO4>H2SO4>H3PO4>H2SiO3,故D正确,
故选D.
点评 本题考查元素周期律的应用,难度不,侧重对基础知识的考查,注意掌握微粒半径比较.


科目:高中化学 来源: 题型:选择题
| A. | 41.8g固体物质为Na2CO3 | |
| B. | 41.8g固体物质为0.1mol Na2CO3和0.4mol Na2O2的混合物 | |
| C. | 41.8g固体物质为31.2g NaHCO3和10.6g Na2CO3的混合物 | |
| D. | 一定量的Na2O2为78g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
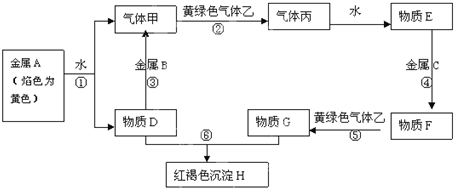
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作及现象 | 实验目的 |
| A | 溶液中滴加盐酸酸化的氯化钡溶液出现白色沉淀 | 检验溶液中存在SO42- |
| B | FeBr2溶液加入少量氯水,溶液有浅绿色变为黄色 | 比较Fe2+、Br-还原性强弱 |
| C | 向一定浓度Na2SiO3溶液中通CO2,溶液变浑浊 | 比较C、Si非金属性强弱 |
| D | 溶液中加KSCN溶液,再加氯水,观察溶液是否出现血红色 | 检验Fe3+溶液中是否含有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2和O3互为同位素 | |
| B. | 在相同的温度与压强下,等体积的O2和O3含有相同的分子数 | |
| C. | 等物质的量的O2和O3含有相同的质子数 | |
| D. | O2和O3的相互转化是物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 它们都是乙烯的同系物 | B. | 它们都属于混合物 | ||
| C. | 它们的分子中都含有C=C双键 | D. | 它们分子中都不含氢原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
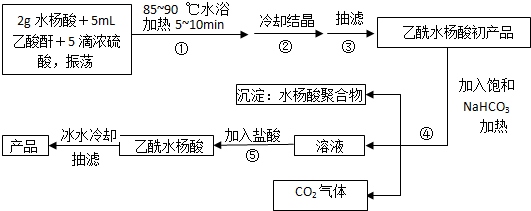
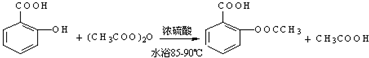 ;反应类型取代反应;
;反应类型取代反应; 、
、 ;
; ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com