
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 苯(苯酚) | 浓溴水 | 过滤 |
| B | 乙酸乙酯(乙酸) | NaOH | 分液 |
| C | CH3CH2OH (H2O) | CaO | 蒸馏 |
| D | 肥皂(甘油) | NaCl | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.苯和苯酚互溶,苯酚能和浓溴水发生取代反应生成溴苯,溴苯和苯能互溶,苯酚和NaOH溶液反应生成可溶性的苯酚钠,苯和氢氧化钠溶液不反应;
B.乙酸乙酯和乙酸都能和NaOH反应,乙酸和饱和碳酸钠反应,乙酸乙酯和饱和碳酸钠溶液不反应;
C.水与CaO反应,增大与乙醇的沸点差异;
D.加NaCl降低肥皂的溶解度,发生盐析.
解答 解:A.苯和苯酚互溶,苯酚能和浓溴水发生取代反应生成溴苯,溴苯和苯能互溶,苯酚和NaOH溶液反应生成可溶性的苯酚钠,苯和氢氧化钠溶液不反应,所以不能用浓溴水除杂,应该用NaOH溶液除杂然后采用分液方法分离,故A错误;
B.乙酸乙酯和乙酸都能和NaOH反应,乙酸和饱和碳酸钠反应,乙酸乙酯和饱和碳酸钠溶液不反应,所以除杂剂应该选取饱和的碳酸钠溶液,然后采用分液方法分离,故B错误;
C.水与CaO反应,增大与乙醇的沸点差异,然后蒸馏可除杂,故C正确;
D.加NaCl降低肥皂的溶解度,发生盐析,然后过滤可除杂,故D正确;
故选AB.
点评 本题考查除杂,为高频考点,把握物质的性质差异性、混合物分离方法为解答的关键,侧重分析与实验能力的考查,除杂时不能引进新的杂质且操作要简便.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应中一定有氧元素参与 | |
| B. | 氧化还原反应中所有元素化合价都变化 | |
| C. | 氧化还原反应只有一种元素的化合价变化 | |
| D. | 氧化还原反应中电子有得必有失,化合价有升必有降 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)3COH的名称:2,2二甲基乙醇 | B. | 乙醛的结构式:CH3CHO | ||
| C. | CH4分子的比例模型: | D. | 聚丙烯的结构简式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
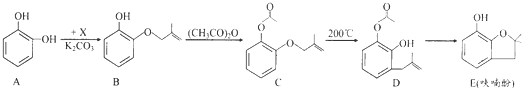
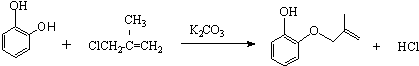 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
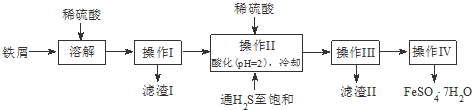
| 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS沉淀完全 | |
| pH值 | 3.9 | 1.6 | 3.0 | 5.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
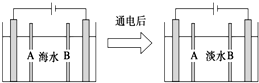
| A. | 阳离子交换膜是A,不是B | |
| B. | 通电后阳极区的电极反应式:2Cl--2e-═Cl2↑ | |
| C. | 工业上阴极使用铁丝网代替石墨碳棒,增大反应接触面 | |
| D. | 阴极区的现象是电极上产生无色气体,溶液中出现少量白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com