
| A. | 氧化还原反应中一定有氧元素参与 | |
| B. | 氧化还原反应中所有元素化合价都变化 | |
| C. | 氧化还原反应只有一种元素的化合价变化 | |
| D. | 氧化还原反应中电子有得必有失,化合价有升必有降 |
分析 A.存在元素化合价变化的反应属于氧化还原反应;
B.反应中可能有多种元素的化合价发生变化;
C.在化学反应中可能所有元素的化合价都发生变化,也可能部分元素的化合价发生变化;
D.氧化还原反应中得失电子守恒.
解答 解:A、存在元素化合价变化的反应属于氧化还原反应,氧化还原反应中不一定有O元素参加,如氢气与氯气的反应,故A错误;
B、2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O反应中各元素的化合价都发生变化;Cl2+H2O=HCl+HClO反应中只有氯元素的化合价变化,故B错误;
C、2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O反应中各元素的化合价都发生变化,有两种元素的化合价发生变化,故C错误;
D、氧化还原反应中得失电子守恒,氧化还原反应中电子有得必有失,化合价有升必有降,故D正确.
故选D.
点评 本题考查了氧化还原反应,难度不大,注意在氧化还原反应中可能同一元素既被氧化又被还原,侧重于基本概念的考查.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤⑥ | B. | ③⑤⑥ | C. | ①③⑤⑥⑦ | D. | ③⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+的水溶液为浅绿色 | |
| B. | Fe3+的水溶液为黄色 | |
| C. | Fe3+具有氧化性,Fe2+具有还原性 | |
| D. | Fe3+溶液中滴入含KSCN-的溶液,立即出现红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
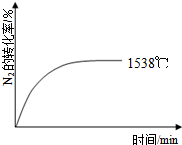 自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.
自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 苯(苯酚) | 浓溴水 | 过滤 |
| B | 乙酸乙酯(乙酸) | NaOH | 分液 |
| C | CH3CH2OH (H2O) | CaO | 蒸馏 |
| D | 肥皂(甘油) | NaCl | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去KCl中混有的KI:溶于水通入过量氯气,蒸发结晶 | |
| B. | 除去BaSO4固体中混有的BaCO3:加过量盐酸后,过滤 | |
| C. | 除去Na2CO3固体中的NaHCO3:加热至恒重 | |
| D. | 除去CO2中混有的HCl:将气体通过饱和Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取用金属钠时,所需用品至少有小刀、镊子、滤纸、玻璃片 | |
| B. | 金属钠与Ca(HCO3)2溶液反应时,既有白色沉淀又有气体逸出 | |
| C. | 生理盐水的质量分数为0.9%,与人体的血液中含量相同,它的溶质是NaCl | |
| D. | Na2O2与碱反应生成盐和水,所以Na2O2是碱性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com