
【题目】现代传感信息技术在化学实验中有广泛的应用.某小组用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理(如图1所示),并测定电离平衡常数Kb. 
(1)实验室可用浓氨水和X固体制取NH3 , X固体可以是
A.生石灰
B.无水氯化钙
C.五氧化二磷
D.碱石灰
(2)检验三颈瓶集满NH3的方法是 .
(3)关闭a,将带有装满水的胶头滴管的橡皮塞塞紧c口, , 引发喷泉实验,电脑绘制三颈瓶内气压变化曲线如图2所示.图2中点时喷泉最剧烈.
(4)从三颈瓶中用(填仪器名称)量取20.00mL氨水至锥形瓶中,用0.05000mol/L HC1滴定.用pH计采集数据、电脑绘制滴定曲线如图3所示.
(5)据图3计算,当pH=11.0时,NH3H2O电离平衡常数Kb近似值,Kb .
【答案】
(1)AD
(2)将湿润的红色石蕊试纸靠近瓶口,试纸变蓝色,证明氨气已收满
(3)打开b,挤压胶头滴管使水进入烧瓶;C
(4)碱式滴定管
(5)1.8×10﹣5
【解析】解:(1)浓氨水易挥发,生石灰、碱石灰溶于水与水反应放出大量的热,能够促进氨气的逸出,而无水氯化钙、五氧化二磷都能够与氨气反应,所以不能用来制氨气;
所以答案是:AD;(2)氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而导致氨水溶液呈碱性,红色石蕊试液遇碱蓝色,
所以答案是:将湿润的红色石蕊试纸靠近瓶口,试纸变蓝色,证明氨气已收满;(3)要形成喷泉实验,应使瓶内外形成负压差,而氨气极易溶于水,所以打开b,挤压胶头滴管使水进入烧瓶,氨气溶于水,使瓶内压强降低,形成喷泉;三颈瓶内气体与外界大气压压强之差越大,其反应速率越快,C点压强最小、大气压不变,所以大气压和C点压强差最大,则喷泉越剧烈,
所以答案是:打开b,挤压胶头滴管使水进入烧瓶;C;(4)氨水显碱性,量取碱性溶液,应选择碱式滴定管;
所以答案是:碱式滴定管;(5)设氨水的物质的量浓度为C,则:C×20mL=0.05000mol/L×22.40mL,解得C(NH3.H2O)=0.056mol/L,弱电解质电离平衡常数Kb= ![]() ;pH=11的氨水中c(OH﹣)=0.001mol/L,c(OH﹣)≈c(NH4+)=0.001mol/L,则:Kb=
;pH=11的氨水中c(OH﹣)=0.001mol/L,c(OH﹣)≈c(NH4+)=0.001mol/L,则:Kb= ![]() =
= ![]() =1.8×10﹣5;
=1.8×10﹣5;
所以答案是:1.8×10﹣5 .
【考点精析】掌握氨的实验室制法是解答本题的根本,需要知道安验室制法:用铵盐与碱共热,2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O.


科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( ) 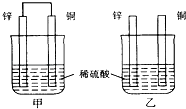
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的氢离子浓度均减小
D.产生气泡的速度甲比乙慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.SiO2 ![]() SiCl4
SiCl4 ![]() Si
Si
B.FeS2 ![]() SO2
SO2 ![]() H2SO4
H2SO4
C.N2 ![]() NH3
NH3 ![]() NH4Cl(aq)
NH4Cl(aq)
D.MgCO3 ![]() MgCl2(aq)
MgCl2(aq) ![]() Mg
Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关碱金属的叙述中,正确的是 ( )
A. 灼烧氯化钾时,火焰没有特殊颜色B. 硝酸铷是离子化合物,易溶于水
C. 在钠、钾、铷三种单质中,铷的熔点最高D. 氢氧化铷是弱碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的表述正确的是( )
A.离子结构示意图 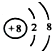 :可以表示16O2﹣ , 也可以表示18O2﹣
:可以表示16O2﹣ , 也可以表示18O2﹣
B.比例模型 ![]() :可以表示甲烷分子,也可以表示四氯化碳分子
:可以表示甲烷分子,也可以表示四氯化碳分子
C.氯化铵的电子式为: ![]()
D.CO2的结构式为:O﹣C﹣O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH.下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH.下列叙述不正确的是( )
A.放电时负极反应为:Zn﹣2e﹣+2OH﹣═Zn(OH)2
B.放电时正极反应为:FeO ![]() +4H2O+3e﹣═Fe(OH)3+5OH﹣
+4H2O+3e﹣═Fe(OH)3+5OH﹣
C.放电时正极附近溶液的碱性增强
D.放电时每转移3mol电子,正极有1molK2FeO4被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,下列物质不能与二氧化硅反应的是( )
①焦炭 ②纯碱 ③碳酸钙 ④氢氟酸 ⑤盐酸 ⑥氢氧化钾 ⑦氧化钙
A. ③⑤⑦ B. ⑤ C. ③⑤ D. ⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2是一种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如图所示: 
部分难溶的电解质溶度积常数(Ksp)如下表:
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10﹣17 | 10﹣17 | 10﹣39 |
已知:一定条件下,MnO4﹣可与Mn2+反应生成MnO2
(1)步骤Ⅱ中消耗0.5molMn2+时,用去1molL﹣1的NaClO3溶液200ml,该反应离子方程式为 .
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是 .
(3)MnO2是碱性锌锰电池的正极材料.放电过程产生MnOOH,该电池正极的电极反应式是 . 如果维持电流强度为5A,电池工作五分钟,理论消耗锌g.(已知F=96500C/mol)
(4)向废旧锌锰电池内的混合物(主要成分MnOOH、Zn(OH)2)中加入一定量的稀硫酸和稀草酸(H2C2O4),并不断搅拌至无CO2产生为止,写出MnOOH参与反应的离子方程式 . 向所得溶液中滴加高锰酸钾溶液产生黑色沉淀,设计实验证明黑色沉淀成分为MnO2
(5)用废电池的锌皮制作ZnSO47H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加入稀H2SO4和H2O2 , 铁溶解变为Fe3+ , 加碱调节pH为时,铁刚好沉淀完全(离子浓度小于1×10﹣5molL﹣1时,即可认为该离子沉淀完全).继续加碱调节pH为时,锌开始沉淀(假定Zn2+浓度为0.1molL﹣1).若上述过程不加H2O2 , 其后果和原因是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是一个化学过程的示意图. 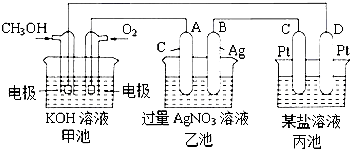
(1)图中乙池是装置.
(2)C(Pt)电极的名称是 .
(3)写出通入CH3OH的电极的电极反应式是 .
(4)乙池中反应的离子方程式为 .
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2mL(标准状况下);此时丙池某电极析出1.6g某金属,则丙中的某盐溶液可能是
A.MgSO4 B.CuSO4 C.NaCl D.CuCl2 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com